题目内容
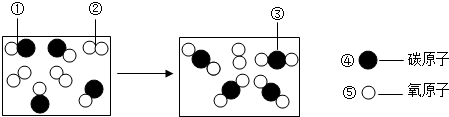
(1)2014年4月10日兰州发生自来水苯(C6H6)含量严重超标事件.检测显示,苯含量均远超出国家限值的10微克/升,最高达20倍.
苯的相对分子质量是 ,苯中碳元素和氢元素的质量之比是 (填最简整数比)
(2)硬水含有较多可溶性钙镁化合物,经常烧硬水的茶壶容易出现水垢.某水垢的成分是CaCO3和Mg(OH)2,为了测定水垢中氢氧化镁的含量,将100g稀盐酸加入20g水垢样品,充分反应后水垢全部消失,并测得反应后剩余物的总质量为115.6g.试计算该水垢中氢氧化镁的质量分数.
苯的相对分子质量是
(2)硬水含有较多可溶性钙镁化合物,经常烧硬水的茶壶容易出现水垢.某水垢的成分是CaCO3和Mg(OH)2,为了测定水垢中氢氧化镁的含量,将100g稀盐酸加入20g水垢样品,充分反应后水垢全部消失,并测得反应后剩余物的总质量为115.6g.试计算该水垢中氢氧化镁的质量分数.
考点:相对分子质量的概念及其计算,元素质量比的计算,根据化学反应方程式的计算
专题:化学式的计算,有关化学方程式的计算
分析:(1)根据苯的化学式为(C6H6),可知其构成,然后利用相对原子质量来计算相对分子质量及元素的质量比.
(2)据此依据化学方程式可计算反应的碳酸钙的质量,进而可求出氢氧化镁的质量分数.
(2)据此依据化学方程式可计算反应的碳酸钙的质量,进而可求出氢氧化镁的质量分数.
解答:解:
(1)根据苯的化学式为(C6H6),则可知:
其相对分子质量为6×12+6×1=78,
其中碳元素和氢元素的质量比为(6×12):(1×6)=12:1,
(2)生成CO2的总质量为:(100g+20g)-115.6g=4.4g;
设:20g水垢中CaCO3的含量为X.
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
X 4.4g
则
=
,解得x=10g
则:水垢中Mg(OH)2的质量分数为:
×100%=50%
故答案为:
(1)78;12:1;(2)50%.
(1)根据苯的化学式为(C6H6),则可知:
其相对分子质量为6×12+6×1=78,
其中碳元素和氢元素的质量比为(6×12):(1×6)=12:1,
(2)生成CO2的总质量为:(100g+20g)-115.6g=4.4g;
设:20g水垢中CaCO3的含量为X.
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
X 4.4g
则
| 100 |
| x |
| 44 |
| 4.4g |
则:水垢中Mg(OH)2的质量分数为:
| 20g-10g |
| 20g |
故答案为:
(1)78;12:1;(2)50%.
点评:本题较简单,学生应充分利用习题信息中笨的化学式结合所学知识来解答.掌握利用化学方程式进行计算的方法步骤.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
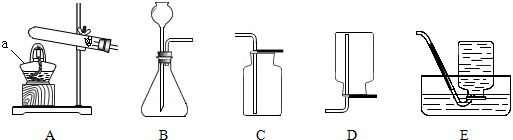
正确的化学实验操作是实验成功和安全的重要保证,下列实验操作正确的是( )
A、 塞紧橡皮塞 |
B、 加热液体 |
C、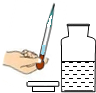 取用液体 |
D、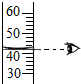 读出液体的体积 |
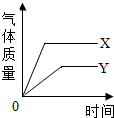 根据金属活动顺序表的有关知识,回答下列问题:
根据金属活动顺序表的有关知识,回答下列问题:
 化学兴趣小组设计的创新实验是“火龙生字”.在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1).用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究:
化学兴趣小组设计的创新实验是“火龙生字”.在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1).用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究: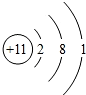 是某粒子的结构示意图,该粒子在化学反应中容易
是某粒子的结构示意图,该粒子在化学反应中容易