题目内容
20.如图是某同学设计的实验室制取二氧化碳并验证其性质的实验装置.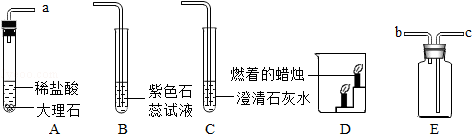
请回答下列问题:
(1)将A、E连接时,应将A装置的导管a与E装置导管的c端相连接.A中发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
(2)将A、B连接,观察到的现象是紫色石蕊试液变红,可验证二氧化碳的性质是CO2+H2O=H2CO3(用化学方程式表示).
(3)将A、C连接,可观察到澄清石灰水变浑浊,反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.
(4)用E收集一瓶二氧化碳气体,取下双孔橡皮塞,将瓶中的气体沿D烧杯左侧内壁缓慢倒入,观察到的现象是燃着的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是二氧化碳的密度比空气大,不燃烧也不支持燃烧.
(5)为计算某大理石中碳酸钙的质量分数,取该大理石10.0g,向其中加入足量的稀盐酸,完全反应后共收集到2.2g二氧化碳气体,计算该大理石中碳酸钙的质量分数.
分析 制取装置包括加热和不需加热两种,实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.将A、B连接,观察到的现象是紫色石蕊试液变红,因为二氧化碳和水反应生成碳酸,碳酸能使紫色变成红色;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳.将瓶中的气体沿D烧杯左侧内壁缓慢倒入,观察到的现象是:燃着的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是:二氧化碳的密度比空气大,不燃烧也不支持燃烧;有关的计算要准确.
解答 解:(1)将A、E连接时,应将A装置的导管a与E装置导管的长管连接,因为二氧化碳的密度比空气大;碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,配平即可;故答案为:c;CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)将A、B连接,观察到的现象是紫色石蕊试液变红,因为二氧化碳和水反应生成碳酸,碳酸能使紫色变成红色;故答案为:紫色石蕊试液变红; CO2+H2O=H2CO3;
(3)二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;故答案为:Ca(OH)2+CO2=CaCO3↓+H2O;
(4)将瓶中的气体沿D烧杯左侧内壁缓慢倒入,观察到的现象是:燃着的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是:二氧化碳的密度比空气大,不燃烧也不支持燃烧;故答案为:燃着的蜡烛自下而上依次熄灭;二氧化碳的密度比空气大,不燃烧也不支持燃烧;
(5)解:设该大理石中碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
x 2.2 g
$\frac{100}{44}=\frac{x}{2.2g}$ 解得x=5.0g
该大理石中碳酸钙的质量分数为$\frac{5.0g}{10.0g}×100%=50%$;
答:该大理石中碳酸钙的质量分数为50%;
故答案为:50%;
点评 本考点主要考查了二氧化碳的性质、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关化学方程式的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 名校课堂系列答案
名校课堂系列答案| A. | 只有硝酸锌和水 | B. | 一定由硝酸锌和硝酸亚铁 | ||
| C. | 一定没有硝酸银 | D. | 如果没有硝酸铜,一定没有硝酸银 |
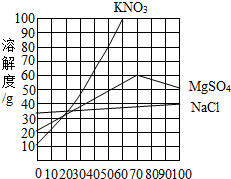 如图是三种物质的溶解度曲线.下列说法错误的是( )
如图是三种物质的溶解度曲线.下列说法错误的是( )| A. | 升高温度,可以使三种物质的溶解度增大 | |
| B. | 降低温度.可以除去饱和KN03溶液中含有的少量NaCl | |
| C. | 50℃时,三种物质的溶解度由大到小的顺序是:KN03>MS04>NaCl | |
| D. | 50℃时,三种饱和溶液降温至10℃,所得溶液溶质的质量分数由大到小的顺序是:NaCl>MgSO4>KNO3 |
| A. | 用向下排空气法收集氧气 | |
| B. | 将集满氧气的集气瓶正放在桌面上 | |
| C. | 收集满氧气后,在水面下用玻璃片盖住瓶口移出水槽 | |
| D. | 收集氧气时,观察到导管口气泡连续均匀放出时开始收集 |
| A. | H2 | B. | O2 | C. | CO2 | D. | NH3 |
(1)填表
| 实验步骤 | 观察到的现象 |
| 在试管中取少量稀盐酸,插入铁丝,充分反应. | 有气泡冒出,溶液由无色变为浅绿色 |
| 在所得的溶液中插入铜丝,充分作用. | 无明显现象 |
| 在所得的溶液中插入铝丝,充分作用. | 铝丝表面有一层黑色物质,溶液由浅绿色变无色 |
(2)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论.小强同学则认为没有必要,只需将小刚同学设计的方案中插入金属的顺序加以调整即可,你认为调整后插入金属的顺序依次为铜、铁、铝.
(3)通过比较、分析,发现上述反应有相似之处:均属于基本反应类型中的置换反应.
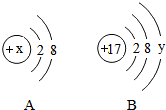 如图A、B分别是某微粒的结构示意图,回答下列问题:
如图A、B分别是某微粒的结构示意图,回答下列问题: