题目内容
4.(一)碳在高温下要使80g氧化铜完全还原,需要碳的质量至少是多少?(请写出详细解题步骤及过程)(二)在实验室里,大红同学用63.2g高锰酸钾加热制取一定质量的氧气后,剩余固体的质量为60g,则在此过程中消耗的高锰酸钾与剩余的高锰酸钾的质量比为1:1.
分析 (一)根据碳在高温时还原氧化铜的反应物和反应条件写出化学反应式即可;根据化学反应式计算碳的质量;
(二)根据化学方程式和氧气的质量求出消耗的高锰酸钾的质量,再求消耗的高锰酸钾与剩余的高锰酸钾的质量比;
解答 (一)解:设使80g氧化铜完全还原,需要碳的质量至少是x
C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
12 160
x 80g
$\frac{12}{x}=\frac{160}{80g}$
x=6g
答:使80g氧化铜完全还原,需要碳的质量至少是6g.
(二)实验中制得氧气的质量为:63.2g-60g=3.2g;
设消耗的高锰酸钾的质量为x,
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 3.2g
$\frac{316}{x}=\frac{32}{3.2g}$
x=31.6g
消耗的高锰酸钾与剩余的高锰酸钾的质量比为:31.6g:(63.2g-31.6g)=1:1;
答案:1:1.
点评 本题考查化学反应式的书写和相关计算,属于基础知识,很好解决,

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列物质常用于改良酸性土壤的是( )
| A. | 烧碱 | B. | 食盐 | C. | 熟石灰 | D. | 大理石 |
12. 中华人民共和国第十二届运动会将于2013年8月31日至2013年9月12日在辽宁省举行,本届全运会设31个大项、40个分项、350个小项.首枚金牌将于5月10日在沈阳进行的竞走决赛中产生.下列有关认识不正确的是( )
中华人民共和国第十二届运动会将于2013年8月31日至2013年9月12日在辽宁省举行,本届全运会设31个大项、40个分项、350个小项.首枚金牌将于5月10日在沈阳进行的竞走决赛中产生.下列有关认识不正确的是( )
 中华人民共和国第十二届运动会将于2013年8月31日至2013年9月12日在辽宁省举行,本届全运会设31个大项、40个分项、350个小项.首枚金牌将于5月10日在沈阳进行的竞走决赛中产生.下列有关认识不正确的是( )
中华人民共和国第十二届运动会将于2013年8月31日至2013年9月12日在辽宁省举行,本届全运会设31个大项、40个分项、350个小项.首枚金牌将于5月10日在沈阳进行的竞走决赛中产生.下列有关认识不正确的是( )| A. | 运动会圣火,作为一种神圣的象征,火的历史可以追溯到史前,燃烧发生的是化学变化 | |
| B. | 火炬中的燃料燃烧会生成水和二氧化碳等物质,这种变化符合质量守恒定律 | |
| C. | 火炬形象是一届运动会的重要标志,也集中体现了办会理念及主办城市特点 | |
| D. | 发展体育事业中利用化学,只要比赛胜利,无需考虑节能、环保、低碳等理念 |
19.以下“家庭小实验”不可行的是( )
| A. | 利用干电池、小灯泡、导线等测溶液的导电性 | |
| B. | 用食醋除去热水瓶中的水垢 | |
| C. | 用洁厕精(主要成分是盐酸)来除去铁锈 | |
| D. | 用过滤的方法把硬水变成软水 |
8.现将10克A和足量B混合加热,A和B发生化学反应,10克A完全反应后生成8克C和4克D.若足量A与4克B完全反应,生成C的质量为( )
| A. | 16克 | B. | 8克 | C. | 4克 | D. | 10克 |

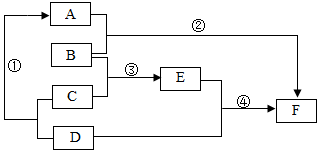 如图是初中化学中六种常见物质之间的转化关系图.
如图是初中化学中六种常见物质之间的转化关系图.