题目内容
14.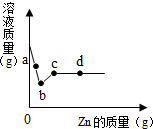 向一定质量AgNO3、Cu(NO3)2和Al(NO3)3的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.
向一定质量AgNO3、Cu(NO3)2和Al(NO3)3的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示. (1)a点溶液中含有的金属离子有哪些?(写离子符号)
(2)b~c(不包括b点)段反应的化学方程式.
(3)d点固体中含有物质(用化学符号表示)?
分析 根据金属与盐溶液的反应进行分析,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,且置换时先把最弱的金属置换出来,并通过各反应的关系进行溶液质量的变化分析
解答 解:在金属活动性顺序中,Al>Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2和Al(NO3)3的混合溶液中加入Zn,与两种溶质依次发生反应
Zn+2AgNO3=Zn(NO3)2+2Ag
65 216
所以析出银的过程是溶液质量减少的过程;
Zn+Cu(NO3)2=Zn(NO3)2+Cu
65 64
所以析出铜的过程是溶液质量增加的过程.
(1)在a点时,硝酸银没有全部参加反应,溶液中含有硝酸银、硝酸铜和生成的硝酸锌,溶质是三种;所以a点溶液中含有的金属离子有Ag+、Cu2+、Zn2+、Al3+;
(2)b~c(不包括b点)段溶液质量增加,所以是锌和硝酸铜反应的过程,反应的化学方程式:Zn+Cu(NO3)2=Zn(NO3)2+Cu;
(3)d点时锌过量,因此d点固体中含有置换出来的银、铜和过量的锌.
故答案为:(1)Ag+Cu2+ Zn2+ Al3+ (2)Zn+Cu(NO3)2=Zn(NO3)2+Cu
(3)Zn Cu Ag
点评 本题考查了金属活动性顺序的应用,要求学生熟悉金属的活动性顺序表,能利用活动性判断反应的发生,还要结合坐标分析各段的意义

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列图标中,属于节约水资源标志的是( )
| A. |  | B. |  | C. |  | D. |  |
19.如表是部分物质的溶解性表(室温),利用表中提供的信息回答下列问题:
(1)NaOH和BaCl2两种物质混合后不能(填“能”或“不能”)发生反应,理由是交换成分没有沉淀、气体或水生成,不符合复分解反应发生的条件.
(2)利用表中阴离子和阳离子构成的物质,写出一个有BaSO4生成的化学方程式BaCl2+Na2SO4═BaSO4↓+2NaCl(合理即可).
| 阴离子 阳离子 | OH- | Cl- | SO42- |
| Na+ | 溶 | 溶 | 溶 |
| Fe2+ | 不 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 |
(2)利用表中阴离子和阳离子构成的物质,写出一个有BaSO4生成的化学方程式BaCl2+Na2SO4═BaSO4↓+2NaCl(合理即可).
2.下列不属于矿物燃料的是( )
| A. | 煤 | B. | 酒精 | C. | 天然气 | D. | 石油 |