题目内容
12. 加碘盐通常在食盐中加碘酸钾(KIO3).如图是超市销售的一种加碘盐标签上的部分文字说明. 请回答下列问题:
加碘盐通常在食盐中加碘酸钾(KIO3).如图是超市销售的一种加碘盐标签上的部分文字说明. 请回答下列问题:(1)碘酸钾中碘元素的化合价为+5
(2)碘酸钾的相对分子质量为?
(3)碘酸钾中钾元素、碘元素和氧元素的原子个数比为1:1:3
(4)碘酸钾中钾元素、碘元素和氧元素的质量比为?
(5)碘酸钾中碘元素的质量分数是?(保留到0.1%).
(6)多少碘酸钾中含碘127mg;
(7)428mg碘酸钾中含碘?
(8)每袋该食盐中碘元素的质量为多少?
(9)中国营养学会推荐:一个18岁的青年每天摄入碘元素的质量为0.15mg.假设碘的来源仅靠这种加碘食盐,该青年每天应摄入这种食盐多少克.(写出计算步骤)
分析 根据已有的化学式的计算进行分析解答即可.
解答 解:(1)碘酸钾中钾元素的化合价为+1,氧元素的化合价为-2,设碘元素的化合价为x,则有:(+1)+x+(-2)×3=0,x=+5,故填:+5;
(2)碘酸钾的相对分子质量为:39+127+16×3=214,故答案为:214;
(3)碘酸钾中钾元素、碘元素和氧元素的原子个数比为1:1:3,故答案为:1:1:3;
(4)碘酸钾中钾元素、碘元素和氧元素的质量比为:39:127:(16×3)=39:127:48,故答案为:39:127:48;
(5)碘酸钾中碘元素的质量分数为:$\frac{127}{214}×100%$≈59.3%,故答案为:59.3%;
(6)碘酸钾中含碘127mg,设碘酸钾的质量为x,x×59.3%=127mg,x=214mg,故答案为:214mg;
(7)428mg碘酸钾中含碘的质量为x,则有:428mg×59.3%=254mg,故答案为:254mg;
(8)每袋该食盐中碘元素的质量为10mg,故答案为:10mg;
(9)根据题意,一个18岁的青年每天摄入碘元素的质量为0.15mg,该加碘盐含碘元素20mg/kg,0.15mg÷20mg∕kg=0.0075kg=7.5g.故答案为:7.5g.
点评 本题考查的是根据化学式的计算,完成此题,可以依据已有的知识结合公式进行.

练习册系列答案
相关题目
7.化学中有许许多多的用“一定”与“不一定”进行的推断,其中推断不正确的是( )
| A. | 最外层电子数为8的粒子一定具有稳定结构,具有稳定结构的粒子最外层电子数不一定是8 | |
| B. | 氧化反应一定属于化合反应,化合反应不一定属于氧化反应 | |
| C. | 加碘食盐的主要成份是氯化钠,氯化钠是由离子构成的 | |
| D. | 氧化物一定含有一种非氧元素 |
4.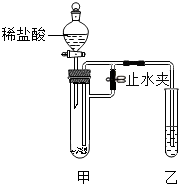 某化学小组在课外活动时做了一个实验,在甲试管中装入某固体物质,乙试管装入某溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).打开止水夹,同时通过分液漏斗加入足量稀盐酸,看到乙试管溶液中有气泡冒出,一段时间后,再关闭止水夹,发现乙中溶液变白色浑浊.符合此实验现象的一组试剂是( )
某化学小组在课外活动时做了一个实验,在甲试管中装入某固体物质,乙试管装入某溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).打开止水夹,同时通过分液漏斗加入足量稀盐酸,看到乙试管溶液中有气泡冒出,一段时间后,再关闭止水夹,发现乙中溶液变白色浑浊.符合此实验现象的一组试剂是( )
 某化学小组在课外活动时做了一个实验,在甲试管中装入某固体物质,乙试管装入某溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).打开止水夹,同时通过分液漏斗加入足量稀盐酸,看到乙试管溶液中有气泡冒出,一段时间后,再关闭止水夹,发现乙中溶液变白色浑浊.符合此实验现象的一组试剂是( )
某化学小组在课外活动时做了一个实验,在甲试管中装入某固体物质,乙试管装入某溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).打开止水夹,同时通过分液漏斗加入足量稀盐酸,看到乙试管溶液中有气泡冒出,一段时间后,再关闭止水夹,发现乙中溶液变白色浑浊.符合此实验现象的一组试剂是( )| 选项 | 甲中固体 | 乙中溶液 |
| A | CaCO3 | Ca(OH)2 |
| B | CuCO3 | NaOH |
| C | Mg | AgNO3 |
| D | KOH | BaCl2 |
| A. | A | B. | B | C. | C | D. | D |
2.小敏用量筒量取液体,将量筒平放且面对刻度平视测量.初次仰视量筒内凹液面的最低处保持水平,读数为45mL,倒出部分液体后,俯视凹液面的最低处,读数为25mL,则该小敏实际倒出液体的体积是( )
| A. | 大于20mL | B. | 小于20mL | C. | 等于20mL | D. | 无法确定 |