题目内容
下列能正确反映对应变化关系的是( )
A、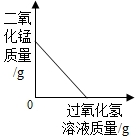 向一定量的二氧化锰中加入过氧化氢溶液 |
B、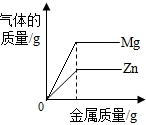 向两份完全相同的稀盐酸中分别不断加入锌、镁 |
C、 将水通电分解 |
D、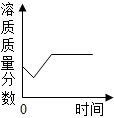 某温度时,向一定量的饱和氢氧化钙溶液中加入少量生石灰,再恢复到原温 |
考点:催化剂的特点与催化作用,电解水实验,溶质的质量分数,金属的化学性质,生石灰的性质与用途
专题:元素化合物知识型
分析:A、过氧化氢在二氧化锰的催化作用下能生成水和氧气,根据催化剂的特点分析;
B、在金属活动性顺序中,位置越靠前的金属与酸反应的速率越快;根据金属的相对原子质量判断产生氢气的多少;
C、根据电解水时产生的氢气和氧气的体积比是2:1分析.
D、根据生石灰和水反应生成氢氧化钙,反应放出热量结合氢氧化钙的溶解度随温度的升高而减小分析.
B、在金属活动性顺序中,位置越靠前的金属与酸反应的速率越快;根据金属的相对原子质量判断产生氢气的多少;
C、根据电解水时产生的氢气和氧气的体积比是2:1分析.
D、根据生石灰和水反应生成氢氧化钙,反应放出热量结合氢氧化钙的溶解度随温度的升高而减小分析.
解答:解:A、向一定量二氧化锰中加入过氧化氢溶液,二氧化锰在反应前后其质量和化学性质保持不变,故A错误;
B、在金属活动性顺序中,镁>锌,镁与酸反应生成氢气的速率大于锌;同时因金属足量,相同质量的酸液完全反应生成氢气的质量相等,故B图象不符合;
C、水通电产生氢气和氧气的体积比是2:1,故C正确;
D、向饱和石灰水中加入少量的生石灰,生石灰和水反应生成氢氧化钙,水少了,原来的饱和溶液要析出一些氢氧化钙固体,又因该反应放出热量,溶液温度升高,氢氧化钙的溶解度随温度的升高而减小,因此一段时间后析出的氢氧化钙固体达到最大值,溶质质量分数达到最小值;随后随着温度的下降,一部分氢氧化钙固体又溶解,溶质质量分数又增加,恢复到原温度时,仍为饱和溶液,同一温度下的物质的饱和溶液,其溶质质量分数相等,故选项错误;
故选C.
B、在金属活动性顺序中,镁>锌,镁与酸反应生成氢气的速率大于锌;同时因金属足量,相同质量的酸液完全反应生成氢气的质量相等,故B图象不符合;
C、水通电产生氢气和氧气的体积比是2:1,故C正确;
D、向饱和石灰水中加入少量的生石灰,生石灰和水反应生成氢氧化钙,水少了,原来的饱和溶液要析出一些氢氧化钙固体,又因该反应放出热量,溶液温度升高,氢氧化钙的溶解度随温度的升高而减小,因此一段时间后析出的氢氧化钙固体达到最大值,溶质质量分数达到最小值;随后随着温度的下降,一部分氢氧化钙固体又溶解,溶质质量分数又增加,恢复到原温度时,仍为饱和溶液,同一温度下的物质的饱和溶液,其溶质质量分数相等,故选项错误;
故选C.
点评:本题考查了常见物质的性质,完成此题,可以依据物质的性质结合具体的图象进行分析.

练习册系列答案
相关题目
三氧化二碳(C2O3)的化学性质与一氧化碳相似.下列关于三氧化二碳的说法错误的是( )
| A、密度比空气小 | B、有毒 |
| C、可以燃烧 | D、具有还原性 |
钛是航空、军工、电力等领域的重要原料.工业上用钛酸亚铁(FeTiO3)冶炼钛(Ti)的过程是:
①2FeTiO3+6C+7Cl2
2TiCl4+2FeCl3+6CO
②在氩气环境中,2Mg+TiCl4
Ti+2MgCl2
下列判断不正确的是( )
①2FeTiO3+6C+7Cl2
| ||
②在氩气环境中,2Mg+TiCl4
| ||
下列判断不正确的是( )
| A、反应②属于置换反应 |
| B、反应②中氯化物的总质量保持不变 |
| C、反应①、②中钛元素的化合价都改变 |
| D、反应②中,氩气只作为保护气并不参加反应 |
化学是一门以实验为基础的学科,以下实验操作中,错误的是( )
| A、向试管内滴加液体时,将胶头滴管伸入试管内 |
| B、用天平称量药品的质量时,应先加大质量的砝码,再加小质量的砝码 |
| C、做细铁丝在氧气中燃烧的实验前,先在集气瓶中加入少量水或铺一层细纱 |
| D、酒精洒在实验桌上燃烧起来,立即用湿抹布盖灭 |
下列做法与社会可持续发展理念相违背的是( )
| A、将工业废水注入地下,治理水污染 |
| B、采用化石燃料除硫技术 |
| C、开发新能源,代替化石燃料 |
| D、推行自行车、公交车等出行方式,减少“碳”排放 |
物质的组成、结构、性质关系归纳错误的是( )
| A、物质由原子、分子、离子等粒子构成 |
| B、元素的化学性质与原子的最外层电子数关系密切 |
| C、原子是化学变化中的最小微粒,因此原子不能再分 |
| D、核内质子数决定了元素的种类 |
下列实验基本操作中,正确的是( )
A、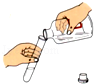 倾倒液体 |
B、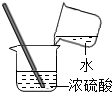 稀释浓硫酸 |
C、 加热液体 |
D、 过滤 |
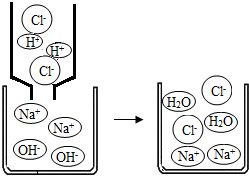 氢氧化钠和稀盐酸能够发生中和反应.
氢氧化钠和稀盐酸能够发生中和反应.