题目内容
16.今有A、B、C、D、E五种装置如图所示.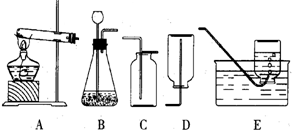
按下列要求回答问题(所选装置用其代号字母表示)
(1)实验室用高锰酸钾的加热分解来制取氧气时,发 生装置选用A,收集装置选用C或E,该装置制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(2)实验室用大理石和稀盐酸来制取二氧化碳时,发生装置选用B,收集装置选用C,该制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)硫化氢是一种无色且有臭鸡蛋气味的气体,能溶于水,可形成一种酸溶液--氢硫酸.实验室用硫化亚铁跟稀硫酸反应制取硫化氢气体.试回答:
①硫化氢气体具有臭鸡蛋气味,这是硫化氢的物理(填“物理”或“化学”)性质.
②硫化氢的水溶液能使石蕊试液变红色.
③实验室制取H2S气体时,发生装置应选用B,收集装置应选用C(填仪器编号).
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室用硫化亚铁(固体)跟稀硫酸反应制取硫化氢气体,因此不需要加热;硫化氢是一种无色且有臭鸡蛋气味的气体,能溶于水,可形成一种酸溶液--氢硫酸,并且密度比空气大,因此只能用向上排空气法收集;有臭鸡蛋气味,这是硫化氢的物理性质,氢硫酸属于酸,因此能使紫色石蕊试液变红色.
解答 解:(1)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;故答案为:A,C或E,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)实验室制取CO2,是在常温下,用实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;故答案为:B,C,CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)实验室用硫化亚铁(固体)跟稀硫酸反应制取硫化氢气体,因此不需要加热;硫化氢是一种无色且有臭鸡蛋气味的气体,能溶于水,可形成一种酸溶液--氢硫酸,并且密度比空气大,因此只能用向上排空气法收集;有臭鸡蛋气味,这是硫化氢的物理性质,氢硫酸属于酸,因此能使紫色石蕊试液变红色;故答案为:物理,红,B,C.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| A. | 浓溶液不一定是饱和溶液,稀溶液一定是不饱和溶液 | |
| B. | 饱和溶液一定是浓溶液,不饱和溶液不一定是稀溶液 | |
| C. | 某一温度下,某物质的饱和溶液浓度要比不饱和溶液的浓度大 | |
| D. | 一定温度下,某物质的饱和溶液中溶解的溶质质量一定比不饱和溶液要多 |
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 石灰水 | D. | 氢氧化钠溶液 |
| A. | 硫酸钠 | B. | 碳酸钠 | C. | 硫酸铜 | D. | 稀硫酸 |
| A. | CO,CO2 | B. | H2,SO2 | C. | H2,CO | D. | CO2 SO2 |
| A. | 硫在氧气中燃烧,发出微弱的淡蓝色火焰 | |
| B. | 棉线在空气中燃烧时,产生烧焦羽毛气味的气体 | |
| C. | 镁条在空气中燃烧,发出耀眼白光 | |
| D. | 红磷在空气中燃烧时,产生大量白色烟雾 |
