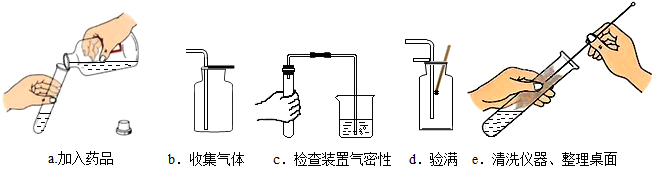
题目内容
17.实验室要配制50g10%的氯化钠溶液,其操作如图所示.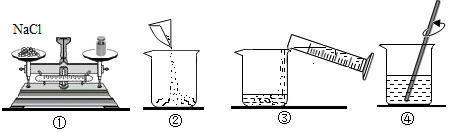
(1)①中称量氯化钠固体的质量为5g,若要配制好的溶液稀释成质量分数为5%的氯化钠溶液,应加水的质量为50g.
(2)下列操作会导致所配溶液的溶质质量分数偏低的是AD(填字母).
A、②中将固体倒入烧杯时洒出 B、③中将水倒入烧杯时洒出
C、溶解完全后,转移时溶液洒出 D、量取所需水时仰视读数.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;溶液稀释前后溶质的质量不变,进行分析解答.
(2)溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大,溶质质量分数变大,则可能是溶质质量偏大或溶剂质量偏小,可以分析出可能造成这两个方面错误的原因进行分析判断即可.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,配制50g10%的氯化钠溶液,需氯化钠的质量=50g×10%=5g.
设要加水的质量为x,根据溶液稀释前后溶质的质量不变,
则50g×10%=(50g+x)×5% x=50g.
(2)A.②中将固体倒入烧杯时洒出,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小.
B.③中将水倒入烧杯时洒出,会造成实际量取的水的体积偏小,则使溶质质量分数偏大.
C.溶液具有均一性,溶解完全后,转移时溶液洒出,溶质质量分数不变.
D.量取水时仰视读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小.
故答案为:(1)5;50;(2)AD.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤(计算、称量、溶解)、注意事项等是正确解答本题的关键.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
13.如图所示是某化学反应的微观示意图,你认为下列说法正确的是( )

| A. | 此反应生成有单质 | |
| B. | 参加反应的两种分子个数比为1:2 | |
| C. | 此反应类型为置换反应 | |
| D. | 反应前后只有H元素化合价没有发生改变 |
9.请你根据提供的实验仪器和药品来参与实验室制取相关气体的实验与研究.实验仪器如下图所示(导管、橡皮塞等未画出).

实验药品:氯酸钾、5%双氧水、大理石、稀盐酸、稀硫酸、高锰酸钾
【比较研究】请填写下表
【实践研究】
(1)某同学选用a、c、d、f、j等仪器组装制取和收集氧气的装置.
①该同学选用的药品是高锰酸钾.
②下面是该同学的部分实验操作,其中不合理的是B、C.
A.先检查装置的气密性,后加药品 B.先固定试管,后放置酒精灯
C.先将导管伸入集气瓶,后加热试管 D.实验结束先将导管移出水面,后熄灭酒精灯
③若用k装置收集氧气,则氧气从m(填“m”或“n”)管通入;检验k装置中收满氧气的方法是将燃着的木条放在n管口,木条燃烧更旺,证明集满.
(2)三位同学根据提供的实验仪器分别设计了下列三套制取和收集二氧化碳的装置.
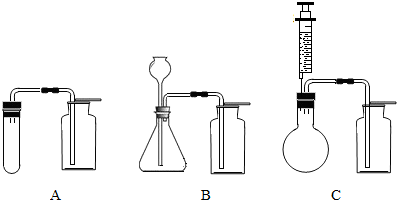
①他们对设计的装置相互进行了交流评价.其中可能收集不到二氧化碳气体的装置是A;
②要检验集气瓶中收集的是否是二氧化碳的方法是向集气瓶中加入澄清石灰水,振荡,溶液变浑浊,证明是二氧化碳.

实验药品:氯酸钾、5%双氧水、大理石、稀盐酸、稀硫酸、高锰酸钾
【比较研究】请填写下表
| 制取气体 | 反应物的状态 | 反应条件 | 收集方法和依据 | |
| 氧气 | 固体 | 加热 | 排水集气法 | O2难溶于水 |
| 二氧化碳 | 固体和液体 | 常温 | 向上排空气法 | 二氧化碳密度比空气大,溶于水 |
(1)某同学选用a、c、d、f、j等仪器组装制取和收集氧气的装置.
①该同学选用的药品是高锰酸钾.
②下面是该同学的部分实验操作,其中不合理的是B、C.
A.先检查装置的气密性,后加药品 B.先固定试管,后放置酒精灯
C.先将导管伸入集气瓶,后加热试管 D.实验结束先将导管移出水面,后熄灭酒精灯
③若用k装置收集氧气,则氧气从m(填“m”或“n”)管通入;检验k装置中收满氧气的方法是将燃着的木条放在n管口,木条燃烧更旺,证明集满.
(2)三位同学根据提供的实验仪器分别设计了下列三套制取和收集二氧化碳的装置.

①他们对设计的装置相互进行了交流评价.其中可能收集不到二氧化碳气体的装置是A;
②要检验集气瓶中收集的是否是二氧化碳的方法是向集气瓶中加入澄清石灰水,振荡,溶液变浑浊,证明是二氧化碳.
7.下列有关微粒的说法正确的是( )
| A. | 分子可分,而原子不可分 | |
| B. | 钠原子得到1个电子形成钠离子 | |
| C. | 过氧化氢分子由氢分子和氧分子组成 | |
| D. | 原子、分子、离子都是构成物质的微粒 |
 如图是某同学在实验室制取和收集气体的装置
如图是某同学在实验室制取和收集气体的装置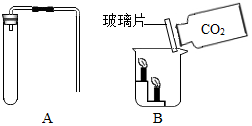 化学兴趣小组的同学设计进行了二氧化碳的制取与性质的实验.
化学兴趣小组的同学设计进行了二氧化碳的制取与性质的实验.