题目内容
6.现有一包固体粉末,可能是碳酸钠、硫酸铜、氯化钠中的一种或几种,为了测定其组成,取适量样品进行下列实验:①取样品溶于水,得到无色澄清溶液;
②取上述溶液适量,滴加氯化钙溶液,出现白色沉淀.
该包粉末中一定含有碳酸钠,可能含有氯化钠.
分析 根据硫酸铜在溶液中显蓝色,碳酸钠和氯化钙会生成白色的碳酸钙沉淀等知识进行分析.
解答 解:硫酸铜在溶液中显蓝色,碳酸钠和氯化钙会生成白色的碳酸钙沉淀,①取样品溶于水,得到无色澄清溶液;所以粉末中一定不含硫酸铜,②取上述溶液适量,滴加氯化钙溶液,出现白色沉淀,所以粉末中一定含有碳酸钠,是否含有氯化钠不会影响实验现象,所以该包粉末中一定含有碳酸钠,可能含有氯化钠.
故答案为:碳酸钠,氯化钠.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
9.属于有机物的是( )
| A. | 甲烷 | B. | 硫酸 | C. | 五氧化二磷 | D. | 碳酸钙 |
1. “皮革水解蛋白”是以废旧皮革制品甚至动物毛发予以“水解”后生成的粉状物质.不法奸商将其混入牛奶,用于提高蛋白质含量,长期食用可能会致癌.为了能够区分牛奶的成分,我们需要学会观察牛奶的标签,如图为某乳品厂生产的奶粉包装袋上部分文字说明,根据说明判断下列说法中正确的是( )
“皮革水解蛋白”是以废旧皮革制品甚至动物毛发予以“水解”后生成的粉状物质.不法奸商将其混入牛奶,用于提高蛋白质含量,长期食用可能会致癌.为了能够区分牛奶的成分,我们需要学会观察牛奶的标签,如图为某乳品厂生产的奶粉包装袋上部分文字说明,根据说明判断下列说法中正确的是( )
 “皮革水解蛋白”是以废旧皮革制品甚至动物毛发予以“水解”后生成的粉状物质.不法奸商将其混入牛奶,用于提高蛋白质含量,长期食用可能会致癌.为了能够区分牛奶的成分,我们需要学会观察牛奶的标签,如图为某乳品厂生产的奶粉包装袋上部分文字说明,根据说明判断下列说法中正确的是( )
“皮革水解蛋白”是以废旧皮革制品甚至动物毛发予以“水解”后生成的粉状物质.不法奸商将其混入牛奶,用于提高蛋白质含量,长期食用可能会致癌.为了能够区分牛奶的成分,我们需要学会观察牛奶的标签,如图为某乳品厂生产的奶粉包装袋上部分文字说明,根据说明判断下列说法中正确的是( )| A. | 此奶粉是纯净物 | B. | 此奶粉中不含任何化学成分 | ||
| C. | 奶粉中的钙.铁.磷.锌指的是单质 | D. | 此袋奶粉中蛋白质的质量为75g |
14.有一包白色粉末可能由CaCO3、Na2SO4、BaCl2、NaCl中的一种或几种组成.把少量该粉末放入足量水中,搅拌、静置、过滤,得到白色固体和滤液.向所得固体中加入稀硝酸,固体溶解并有气体放出.向所得溶液中加入稀硫酸,有白色固体生成.该粉末中肯定没有的物质是( )
| A. | CaCO3 | B. | Na2SO4 | C. | BaCl2 | D. | NaCl |
1.某无色气体由CH4、H2、CO和CO2中的某种或某几种气体组成.将此气体通过过量的澄清石灰水出现浑浊.把剩余气体导出后在空气中点燃,在火焰上方罩一干燥的烧杯足够的时间,没有水雾生成.则原混合气体的成分是( )
| A. | CO2和CO | B. | H2和CO2 | C. | CH4和H2 | D. | CO、CO2和H2 |
11.向下列物质中分别加入足量的蒸馏水,搅拌后能形成无色溶液的是( )
| A. | 面粉 | B. | 氯化铜 | C. | 食盐 | D. | 食用油 |
18.不另选试剂,仅利用组内物质之间的相互反应,就能鉴别出来的是( )
| A. | CuSO4 NaOH HCl H2SO4 | B. | CaCl2 KNO3 Na2CO3 Na2SO4 | ||
| C. | Ca(OH)2 HCl NaCl HNO3 | D. | BaCl2 Na2SO4 Na2CO3 HCl |
15.能供给呼吸的气体是( )
| A. | 氧气 | B. | 氮气 | C. | 稀有气体 | D. | 二氧化碳 |
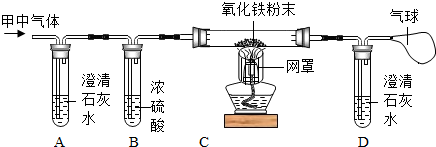 某兴趣小组的同学在甲、乙两个充满O2的密闭容器中各加入一定量的碳粉,在高温条件下使其充分反应,待反应结束后,两个容器中的碳粉都已完全消失.该小组成员对两容器中反应后的气体进行如下探究:
某兴趣小组的同学在甲、乙两个充满O2的密闭容器中各加入一定量的碳粉,在高温条件下使其充分反应,待反应结束后,两个容器中的碳粉都已完全消失.该小组成员对两容器中反应后的气体进行如下探究: