题目内容
过氧化钠(Na2O2)是一种浅黄色的固体,常温下能与二氧化碳反应生成氧气:2Na2O2+2CO2═2Na2CO3+O2某学生以石灰石、稀盐酸和过氧化钠为原料制取氧气,设计出如图实验装置,请你按下列要求回答:
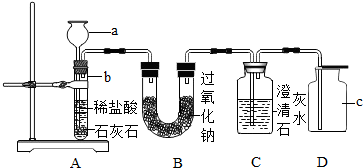
(1)标号为a、b、c的仪器名称:a 、b 、c ;
(2)A装置中反应的化学方程式是: ;
(3)检验D装置中是否收集满氧气的方法是: .

(1)标号为a、b、c的仪器名称:a
(2)A装置中反应的化学方程式是:
(3)检验D装置中是否收集满氧气的方法是:
考点:二氧化碳的实验室制法,气体的净化(除杂),氧气的检验和验满,书写化学方程式、文字表达式、电离方程式
专题:综合实验题
分析:(1)根据仪器名称解答;
(2)碳酸钙与稀盐酸反应生成氯化钙和水和二氧化碳,写出反应的化学方程式;
(3)用带火星的木条去验满氧气.
(2)碳酸钙与稀盐酸反应生成氯化钙和水和二氧化碳,写出反应的化学方程式;
(3)用带火星的木条去验满氧气.
解答:解:(1)标号为a、b、c的仪器:长颈漏斗,试管,集气瓶;
(2)碳酸钙与稀盐酸反应生成氯化钙和水和二氧化碳,反应的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)检验D装置中是否收集满氧气的方法是:用带火星的木条放在集气瓶口,木条复燃则已满.
答案:(1)长颈漏斗;试管;集气瓶;
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)用带火星的木条放在集气瓶口,木条复燃则已满.
(2)碳酸钙与稀盐酸反应生成氯化钙和水和二氧化碳,反应的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)检验D装置中是否收集满氧气的方法是:用带火星的木条放在集气瓶口,木条复燃则已满.
答案:(1)长颈漏斗;试管;集气瓶;
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)用带火星的木条放在集气瓶口,木条复燃则已满.
点评:是对气体制取装置,收集装置以及常见气体性质等考查,考查内容简单注重基础.

练习册系列答案
相关题目