题目内容
在一个密闭容器内有A.B.C.D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表,试推断该容器中发生的化学反应基本类型为( )
| 物质 | A | B | C | D |
| 反应前质量/g | 2 | 2 | 32 | 5 |
| 反应后质量/g | 待测 | 20 | 0 | 12 |
| A、化合反应 | B、分解反应 |
| C、置换反应 | D、复分解反应 |
考点:质量守恒定律及其应用,反应类型的判定
专题:化学用语和质量守恒定律
分析:反应后B质量增加18g,是生成物;
反应后C质量减少32g,是反应物;
反应后D质量增加7g,是生成物;
根据质量守恒定律可知,A是生成物,生成的质量为:32g-18g-7g=7g.
反应后C质量减少32g,是反应物;
反应后D质量增加7g,是生成物;
根据质量守恒定律可知,A是生成物,生成的质量为:32g-18g-7g=7g.
解答:解:该反应中,反应后C物质质量增加,是反应物;
反应后A物质质量增加,是生成物;
反应后B物质质量增加,是生成物;
反应后D物质质量增加,是生成物;
该反应中,反应物是一种,生成物是三种,属于分解反应.
故选:B.
反应后A物质质量增加,是生成物;
反应后B物质质量增加,是生成物;
反应后D物质质量增加,是生成物;
该反应中,反应物是一种,生成物是三种,属于分解反应.
故选:B.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断反应类型、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
相关题目
空气中含量最多的元素和地壳中含量第二的金属元素及人体中含量最多的元素,共同组成化合物,其化学式可能为( )
| A、Al(NO3)3 |
| B、Fe(NO3)3 |
| C、Fe2O3 |
| D、Fe(NO3)2 |
 已知KMnO4与浓HCl在常温下反应能产生Cl2,黄绿色易溶于水的氯气有毒性,并能与氢氧化钠溶液反应.若用图示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应.每个虚线框表示一个单元装置,其中存在明显错误的是(不考虑①单元装置)( )
已知KMnO4与浓HCl在常温下反应能产生Cl2,黄绿色易溶于水的氯气有毒性,并能与氢氧化钠溶液反应.若用图示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应.每个虚线框表示一个单元装置,其中存在明显错误的是(不考虑①单元装置)( )| A、只有④处 |
| B、只有②处 |
| C、只有②和③处 |
| D、②、③、④处 |
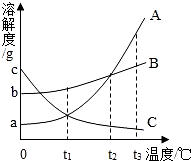 如图所示是A、B、C三种固体物质的溶解度曲线.下列说法正确的是( )
如图所示是A、B、C三种固体物质的溶解度曲线.下列说法正确的是( )| A、在t1℃时,A、B两种物质饱和溶液的溶质质量分数相等 |
| B、在t3℃时,若10g水最多能溶解3g B物质,则10g水最多能溶解A物质的质量小于3g |
| C、三种物质的溶解度关系为B>A>C时的温度为t℃,则t的取值范围是t1<t<t2 |
| D、将A、B、C三种物质的饱和溶液从t2℃降温到t1℃时,溶质质量分数保持不变的是A和B |
下列关于氧气的说法,不科学的是( )
| A、常用带火星的木条来检验空气中的O2 |
| B、空气中的氧气主要来自于植物的光合作用 |
| C、用含有氧元素的物质反应才有可能产生氧气 |
| D、自然界的水中含有一定量的氧气 |
下面是对“2”的含义的解释,其中错误的是( )
| A、Fe2+:一个亚铁离子带2个单位正电荷 |
| B、Ba(OH)2:氢氧化钡中,钡离子和氢氧根离子的个数比是1:2 |
| C、Mg2+:带2个单位正电荷的镁离子 |
| D、2SO42-:2个硫酸根离子,每个硫酸根离子带2个单位负电荷 |
如图为初中化学常见气体的发生装置与收集装置,有关这些装置的说法不正确的是( )
A、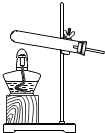 如图装置可作为加热固体制取气体的发生装置 |
B、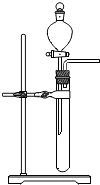 如图装置中分液漏斗的作用是方便添加液体药品 |
C、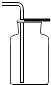 如图装置可用于收集H2、CO2 |
D、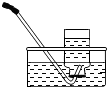 如图装置可用于收集H2、O2 |