题目内容
9.已调平的托盘天平两边个放一个质量相等的烧杯,向烧杯中各倒入质量相等、质量分数也相等的稀硫酸,然后在左盘的烧杯中放入一定质量的金属X粉末,同时在右盘的烧杯中加入与X金属质量相等的Y金属粉末.观察到天平的指针先偏向左边,当两种金属完全溶解后,天平的指针偏向右边.则X、Y可能是下列组合中的( )| 金属 | A | B | C | D |
| X | Mg | Zn | Fe | Zn |
| Y | Fe | Mg | Zn | Fe |
| A. | A | B. | B | C. | C | D. | D |
分析 烧杯中的硫酸足量,因此反应产生氢气的多少决定于金属的质量;金属与酸反应放出氢气,使天平两端质量减小,金属活动性越强,与酸反应生成氢气速率越快;由于等质量的金属完全反应放出氢气质量不同,因此,两端金属完全反应后天平仍不能平衡;因此,需要根据天平指针的偏向,确定金属的活动性及等质量金属完全反应放出氢气质量的大小,判断两种金属.
解答 解:开始时天平的指针先偏向左边,说明天平左边质量减少地较慢,即Y与酸反应比X剧烈,金属Y活动性比X的活动性强;金属Mg、Fe、Zn的活动性从强到弱的顺序为:Mg>Zn>Fe;最后偏向右边,说明到反应结束时,左边产生气体较多,即等质量金属完全反应Y产生氢气的量小于X;等质量的Mg、Fe、Zn与足量的酸完全反应产生氢气质量从大到小的顺序为:Mg>Fe>Zn;综上所述只有C符合.
故选:C.
点评 本题考查了金属与酸反应的速度和产生的氢气质量关系,完成此题,要根据金属活动性顺序的意义和金属与酸的反应条件.

练习册系列答案
相关题目
20.将稀硫酸中加入氧化铜和铁粉的混合物,进行反应,当反应停止后,滤出不溶物,并向滤液中投入一枚小铁钉,一会儿后取出,发现铁钉表面出现红色物质,则可推得( )
| A. | 滤液中一定含有硫酸亚铁,一定不含有硫酸铜 | |
| B. | 滤液中一定含有硫酸亚铁,但是不一定含有硫酸铜 | |
| C. | 不溶物中一定含有铁 | |
| D. | 硫酸一定没有剩余 |
17.有NaCl、MgCl2、FeCl3三种溶液,分别与AgNO3溶液反应,生成的AgCl沉淀的质量刚好相等,则消耗溶质AgNO3的质量比是( )
| A. | 1:2:3 | B. | 3:2:1 | C. | 2:3:6 | D. | 1:1:1 |
14.在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上附粘附着白色物质.
【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】甲认为黑色颗粒是碳,白色物质可能是Na2O或Na2CO3或Na2O与Na2CO3或这两种物质的混合物;
乙同学也认为黑色颗粒是碳,但白色物质是氢氧化钠.
甲同学立刻认为乙同学的猜想有错误,其理由是反应物中无氢元素.
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O=2NaOH
实验探究】甲同学对白色物质进行实验探究.
【反思评价】丙同学认为方案1得到的结论不正确,理由是Na2CO3溶液显碱性,也会使酚酞变红.
【得出结论】钠在二氧化碳中燃烧的化学方程式为4Na+3CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】甲认为黑色颗粒是碳,白色物质可能是Na2O或Na2CO3或Na2O与Na2CO3或这两种物质的混合物;
乙同学也认为黑色颗粒是碳,但白色物质是氢氧化钠.
甲同学立刻认为乙同学的猜想有错误,其理由是反应物中无氢元素.
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O=2NaOH
实验探究】甲同学对白色物质进行实验探究.
| 实验方案 | 实 验 操 作 | 实验现象 | 结 论 |
| 方案1 | 取样品少量于试管中,加入适量水,振荡,样品 全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质 为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质 是Na2CO3 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
【得出结论】钠在二氧化碳中燃烧的化学方程式为4Na+3CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
1.下列标志中,用来提醒人们注意节约用水的是( )
| A. |  | B. |  | C. |  | D. |  |
1.下列物质间的转化不能都通过一步反应实现的是( )
| A. | Fe→FeCl3→Cu | B. | NaOH→H2O→Ca(OH)2 | C. | O2→H2O→O2 | D. | CuSO4→Cu→CuO |
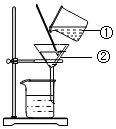 (1)写出仪器名称①烧杯②漏斗.
(1)写出仪器名称①烧杯②漏斗.