题目内容
1.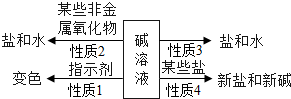 请结合小明同学对碱的四点化学性质的归纳图完成下列问题.(箭头上方的物质是指与碱反应的物质)
请结合小明同学对碱的四点化学性质的归纳图完成下列问题.(箭头上方的物质是指与碱反应的物质)①碱溶液能使无色酚酞溶液变红.
②澄清的石灰水长期暴露在空气中会变质的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O,所以澄清的石灰水必须密封保存(或要使用澄清的石灰水时必须用新制).
③请帮小明补充完整性质3箭头上方的反应物质是酸(填“酸”或“碱”或“盐”).
④碱溶液有相似的化学性质,是因为碱溶液中都含有OH-(填化学符号).
分析 根据已有的碱的性质以及化学方程式的书写的知识进行分析解答即可.
解答 解:①碱溶液能使无色酚酞溶液变红,故填:红.
②澄清的石灰水长期暴露在空气中会变质是因为氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,其化学方程式为 Ca(OH)2+CO2═CaCO3↓+H2O,所以澄清的石灰水必须密封保存,故填:Ca(OH)2+CO2═CaCO3↓+H2;密封.
③碱能与酸反应生成盐和水,故填:酸.
④碱溶液有相似的化学性质,是因为碱溶液中都含有氢氧根离子,故填:OH-.
点评 本题考查的是常见的碱的性质,完成此题,可以依据已有的知识进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.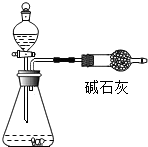 同学们想测定一定质量的石灰石中CaCO3质量分数,他们设计了如图的实验装置(碱石灰的成分是CaO和NaOH的混合物),利用测定碱石灰质量增加来计算碳酸钙的质量.
同学们想测定一定质量的石灰石中CaCO3质量分数,他们设计了如图的实验装置(碱石灰的成分是CaO和NaOH的混合物),利用测定碱石灰质量增加来计算碳酸钙的质量.
(1)该装置导致实验结果偏大的可能原因是BCD.
A.装置内残留的CO2气体不能全部排出.
B.产生的CO2气体中混有氯化氢气体,同时被碱石灰吸收.
C.产生的CO2气体中混有水蒸气,同时被碱石灰吸收.
D.球形干燥管与空气相通,也会吸收空气中的CO2和H2O.
(2)做完上述实验后,同学们对反应后反应器内的剩余溶液的溶质成分产生了兴趣,他们继续进行了以下实验探究:将剩余的溶液倒入烧杯中,微热后冷却到室温.
上表甲、乙、丙三个同学的实验操作中有错误的是丙(选填“甲”“乙”或“丙”)同学的方案.
 同学们想测定一定质量的石灰石中CaCO3质量分数,他们设计了如图的实验装置(碱石灰的成分是CaO和NaOH的混合物),利用测定碱石灰质量增加来计算碳酸钙的质量.
同学们想测定一定质量的石灰石中CaCO3质量分数,他们设计了如图的实验装置(碱石灰的成分是CaO和NaOH的混合物),利用测定碱石灰质量增加来计算碳酸钙的质量.(1)该装置导致实验结果偏大的可能原因是BCD.
A.装置内残留的CO2气体不能全部排出.
B.产生的CO2气体中混有氯化氢气体,同时被碱石灰吸收.
C.产生的CO2气体中混有水蒸气,同时被碱石灰吸收.
D.球形干燥管与空气相通,也会吸收空气中的CO2和H2O.
(2)做完上述实验后,同学们对反应后反应器内的剩余溶液的溶质成分产生了兴趣,他们继续进行了以下实验探究:将剩余的溶液倒入烧杯中,微热后冷却到室温.
| 实验操作 | 实验现象 | 实验结论 | |
甲同学 | 取烧杯中溶液少许于试管中,向其中滴加紫色石蕊试液 | 现象:溶液变为红色 | 溶液显酸性(含有H+);溶质中有氯化氢. |
乙同学 | 取烧杯中溶液少许于试管中,向其中加入少量锌粒 | 现象:产生气泡,反应的化学方程式是: Zn+2HCl═ZnCl2+H2↑ | |
丙同学 | 取烧杯中溶液少许于试管中,向其中加入少量硝酸银溶液 | 现象:产生白色沉淀 |
9.在一密闭容器中,有甲,乙,丙,丁四种物质在一定条件下充分反应,测得反应前后各物质的质量如表所示:( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 4 | 2 | 58 | 5 |
| 反应后质量/g | 待测 | 27 | 0 | 19 |
| A. | 分解反应 | B. | 化合反应 | C. | 氧化反应 | D. | 不能确定 |
6.物质的名称与化学式相应均正确的一组是( )
| A. | 氧气 O3 | B. | 氯化镁 MgCl2 | C. | 氧化铁O4Fe3 | D. | 碳酸钠NaCO3 |
10.下列说法中正确的是( )
| A. | 橡胶、纤维、塑料都是合成有机高分子材料 | |
| B. | 用水可以灭火,因为水可以降低可燃物的着火点 | |
| C. | 为增加肥效,把硝酸铵和草木灰混合使用 | |
| D. | 气味能闻得到却看不到,说明分子很小 |
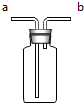 如图有多种功能,如手机气体,洗涤气体等.回答下列问题:
如图有多种功能,如手机气体,洗涤气体等.回答下列问题: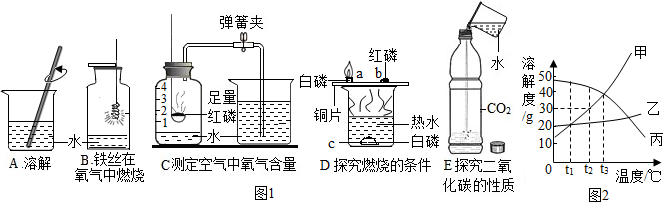
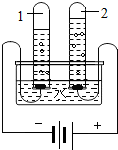 水是重要的自然资源,我们应该了解有关水的一些知识.
水是重要的自然资源,我们应该了解有关水的一些知识.