题目内容
用5000t 含Fe2O370%的赤铁矿石,理论上可以炼出含铁96%的生铁质量是( )
| A、3500t | B、2450t | C、2552.1t | D、2606.8t |
分析:可利用CO还原氧化铁的反应化学方程式,由参加反应的氧化铁的质量计算可生成铁的质量,铁的质量与生铁中铁的含量之比可求得理论上可以炼出含铁96%的生铁质量.
解答:解:设理论上可以炼出含铁96%的生铁质量为x
5000t 含Fe2O370%的赤铁矿石中氧化铁的质量=5000t×70%=3500t,炼出的生铁中铁的质量为x×96%;
Fe2O3+3CO
2Fe+3CO2
160 112
3500t x×96%
=
x=2552.1t
故选C.
5000t 含Fe2O370%的赤铁矿石中氧化铁的质量=5000t×70%=3500t,炼出的生铁中铁的质量为x×96%;
Fe2O3+3CO
| ||
160 112
3500t x×96%
| 160 |
| 3500t |
| 112 |
| x×96% |
x=2552.1t
故选C.
点评:根据化学方程式进行计算时,所使用的质量均为纯净物的质量,不能把不纯物质的质量直接代入化学方程式进行计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
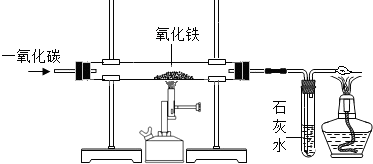 铁及其化合物在日常生活中随处可见.
铁及其化合物在日常生活中随处可见.