题目内容
12.如图是实验室常用的一些装置,请按要求回答有关问题.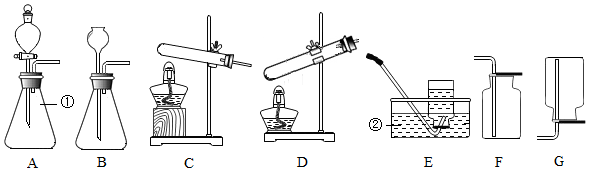
(1)写出带标号仪器的名称:①锥形瓶;②水槽;
(2)用排空气法收集氢气时选用的气体收集装置是G,选择的依据是氢气的密度比空气小.
(3)若实验时采用加热 高锰酸钾的方法制取氧气,需要选择装置C与E连接,则该装置中反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(4)A装置采用分液漏斗代替长颈漏斗来进行分解过氧化氢制取氧气的实验,其优点在于:可以控制加入过氧化氢溶液的速度.
分析 锥形瓶是常用的反应容器,水槽是常用的盛水的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.A装置采用分液漏斗代替长颈漏斗来进行分解过氧化氢制取氧气的实验,其优点在于:可以控制加入过氧化氢溶液的速度.
解答 解:(1)锥形瓶是常用的反应容器,水槽是常用的盛水的仪器,故答案为:锥形瓶;水槽;
(2)氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集,故答案为:G;氢气的密度比空气小;
(3)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:C;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)A装置采用分液漏斗代替长颈漏斗来进行分解过氧化氢制取氧气的实验,其优点在于:可以控制加入过氧化氢溶液的速度;故答案为:可以控制加入过氧化氢溶液的速度;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
2.关于一氧化碳和二氧化碳的叙述正确的是( )
| A. | 一氧化碳和二氧化碳均有可燃性 | |
| B. | 一氧化碳和二氧化碳均有毒 | |
| C. | 一氧化碳和二氧化碳均有还原性 | |
| D. | 固体的二氧化碳叫“干冰”,可用于人工降雨 |
20.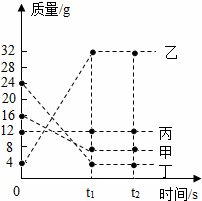 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )| A. | 该反应中,乙、丁的质量变化之比为7:5 | |
| B. | 该反应为化合反应 | |
| C. | 该反应中,甲、乙的质量变化之比为1:4 | |
| D. | 丙可能为该反应的催化剂 |
 如图是密闭体系中某反应的微观示意图,“
如图是密闭体系中某反应的微观示意图,“ ”和“
”和“ ”分别表示不同原子,请回答下列问题.
”分别表示不同原子,请回答下列问题. D.
D.