题目内容
18.如图是常见的气体发生装置和收集装置.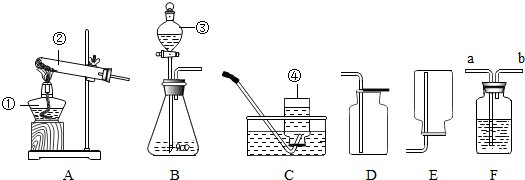
(1)写出①和③所指仪器的名称:①酒精灯;③分液漏斗;
(2)实验室用高锰酸钾制取氧气的发生装置可以选用A(填字母),实验室用高锰酸钾制取氧气的发生装置可以选用但是要在试管口放一团蓬松的棉花,作用是防止高锰酸钾进入导管.该反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+2O2↑.
(3)实验室用无水醋酸钠固体和固体碱石灰加热制取甲烷气体.甲烷的密度比空气小,
不溶于水.则收集甲烷时可选用的装置为C或E(填字母).
(4)如图F是某学生设计的一种有洗气、贮气等用途的装置. 欲除去02中混有的水蒸气,瓶中可盛浓硫酸:氢气是难溶于水的气体,当用排水集气法收集氢气时,瓶内先装满水,气体从b(填“a”或“b”,下同)处导管通入.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
(3)发生装置的选择要根据反应物的状态和反应条件,收集装置要根据气体的密度和溶水性;
(4)可以根据装置的特点方面进行分析、判断,从而判断出气体的进入途径,浓硫酸具有吸水性,排水法收集氢气时要短进,长出.
解答 解:(1)①是酒精灯,常用作热源;③是分液漏斗,通过分液漏斗可以向反应容器中注入液体药品.
故填:酒精灯;分液漏斗;
(2)实验室用高锰酸钾制取氧气需要加热,发生装置可以选用A装置;要在试管口放一团蓬松的棉花,作用是防止高锰酸钾进入导管;反应的方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+2O2↑
故填:A、高锰酸钾进入导管、2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+2O2↑;
(3)实验室用无水醋酸钠固体和固体碱石灰加热制取甲烷气体,反应需加热,发生装置选择A;甲烷的密度比空气小,不溶于水,发生装置选择C或E.
故填:C、E;
(4)浓硫酸具有吸水性,可用作干燥剂,所以欲除去O2中混有的水蒸气,瓶中可盛浓硫酸;故填:浓硫酸;
当用排水集气法收集氢气时,瓶内先装满水,气体应该从b处导管通入,这样水从a处导管排出,如果氢气从a处导管通入时,不能收集到氢气.故填:b;
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下表是部分元素的有关信息.请根据表中的信息回答问题:
(1)上表中共有2种金属元素,硫化氢的化学式是H2S.
(2)上表中化学性质相似的元素是Cl和Br(填元素符号);
(3)氯离子的最外层电子数是8.
(4)从上表中可以看出元素的化合价与最外层电子数存在着关系,其中的关系是删掉:元素的最高正价=最外层电子数;非金属元素的负价=最高正价-8.
| 元素名称及符号 | 钠Na | 镁Mg | 硫S | 氯Cl | 溴Br | |
| 最外层电子数 | 1 | 2 | 6 | 7 | 7 | |
| 常 见 化合价 | 最高正价 | +1 | +2 | +6 | +7 | +7 |
| 负价 | 无 | 无 | -2 | -1 | -1 | |
(2)上表中化学性质相似的元素是Cl和Br(填元素符号);
(3)氯离子的最外层电子数是8.
(4)从上表中可以看出元素的化合价与最外层电子数存在着关系,其中的关系是删掉:元素的最高正价=最外层电子数;非金属元素的负价=最高正价-8.
3.“氯化铁溶液中含有铁离子、氯离子和水分子等微粒,是什么微粒使氯化铁溶液呈黄色的呢?”为推断氯化铁溶液呈黄色的微粒是什么,他们第一步观察了蒸馏水的颜色为无色,第二步观察了氯化钠和氯化钾溶液,发现俩溶液均为无色.后一步观察,他们是为了证明( )
| A. | 氯离子是无色的 | B. | 铁离子是黄色的 | C. | 钠离子是无色的 | D. | 钾离子是无色的 |
