题目内容
下列实验方案中,能达到目的是( )
| A、比较金属活动性强弱:将等质量的铁丝和锌粒放入等浓度的稀盐酸中 |
| B、制取Fe(OH)3:将Ba(OH)2溶液和Fe2(SO4)3溶液混合后过滤 |
| C、除去H2中的HCl气体和H2O:将混合气体依次通过NaOH溶液和浓硫酸 |
| D、分离BaCl2和NaCl的混合溶液:加适量NaOH溶液,充分反应后过滤 |
考点:化学实验方案设计与评价,常见气体的检验与除杂方法,金属活动性顺序及其应用,碱的化学性质,盐的化学性质
专题:简单实验方案的设计与评价
分析:A、根据铁丝和锌粒都和盐酸反应放出氢气进行解答;
B、根据氢氧化钡溶液和硫酸铁溶液反应生成氢氧化铁沉淀和硫酸钡沉淀进行解答;
C、根据氢氧化钠溶液能和氯化氢气体反应,浓硫酸具有吸水性,且二者都不和氢气反应进行解答;
D、根据BaCl2和NaCl与NaOH溶液都不反应,且氯化钡和氯化钠都溶于水进行解答.
B、根据氢氧化钡溶液和硫酸铁溶液反应生成氢氧化铁沉淀和硫酸钡沉淀进行解答;
C、根据氢氧化钠溶液能和氯化氢气体反应,浓硫酸具有吸水性,且二者都不和氢气反应进行解答;
D、根据BaCl2和NaCl与NaOH溶液都不反应,且氯化钡和氯化钠都溶于水进行解答.
解答:解:A、铁丝和锌粒都和盐酸反应放出氢气,所以将等质量的铁丝和锌粒放入等浓度的稀盐酸中不能比较金属活动性强弱,故A错误;
B、氢氧化钡溶液和硫酸铁溶液反应生成氢氧化铁沉淀和硫酸钡沉淀,所以将Ba(OH)2溶液和Fe2(SO4)3溶液混合后过滤不能制取Fe(OH)3,故B错误;
C、氢氧化钠溶液能和氯化氢气体反应,浓硫酸具有吸水性,且二者都不和氢气反应,所以将混合气体依次通过NaOH溶液和浓硫酸能除去H2中的HCl气体和H2O,故C正确;
D、BaCl2和NaCl与NaOH溶液都不反应,且氯化钡和氯化钠都溶于水,所以不能用加适量NaOH溶液,充分反应后过滤的方法分离BaCl2和NaCl的混合溶液,故D错误.
故选:C.
B、氢氧化钡溶液和硫酸铁溶液反应生成氢氧化铁沉淀和硫酸钡沉淀,所以将Ba(OH)2溶液和Fe2(SO4)3溶液混合后过滤不能制取Fe(OH)3,故B错误;
C、氢氧化钠溶液能和氯化氢气体反应,浓硫酸具有吸水性,且二者都不和氢气反应,所以将混合气体依次通过NaOH溶液和浓硫酸能除去H2中的HCl气体和H2O,故C正确;
D、BaCl2和NaCl与NaOH溶液都不反应,且氯化钡和氯化钠都溶于水,所以不能用加适量NaOH溶液,充分反应后过滤的方法分离BaCl2和NaCl的混合溶液,故D错误.
故选:C.
点评:本题难度不大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、目前世界年产量最高的金属是铝 |
| B、把生铁炼成钢就是把生铁中的杂质全部除去,使其变为纯铁 |
| C、世界上每年因腐蚀而报废的金属材料和设备相当于年产量的20%-40% |
| D、金属铁、铝、铜均具有银白色的金属光泽 |
某化学兴趣小组为测定Fe、Cu、Ag三种金属的活动性顺序设计了四种方案,每种方案所需试剂如下,你认为不可行的是( )
| A、Cu、Ag、FeSO4溶液 |
| B、Fe、Ag、CuSO4溶液 |
| C、Fe、Cu、稀盐酸、AgNO3溶液 |
| D、Cu、FeCl2溶液、AgNO3溶液 |
下列反应不是置换反应的是( )
A、H2+CuO
| ||||
B、CO+CuO
| ||||
C、3C+2Fe2O3
| ||||
| D、Mg+2HCl═MgCl2+H2↑ |
某铅酸蓄电池用的是28%的稀硫酸,现用1.0kg 98%的浓硫酸配制该稀硫酸.下列说法中正确的是( )
| A、配制该稀硫酸时,把水沿容器内壁缓慢注入浓硫酸中 |
| B、用1.0kg 98%的浓硫酸可配制3.5kg 28%的稀硫酸 |
| C、配制好的稀硫酸可以存放在铁制容器中 |
| D、28%的稀硫酸中溶质与溶剂的质量比为28:100 |
某物质在氧气中燃烧后只生成水和二氧化碳,关于该物质的组成,下列说法中正确的是( )
| A、一定含有C、H、O三种元素 |
| B、一定含有C、H元素,不含O元素 |
| C、一定含有C、H元素,可能含有O元素 |
| D、可能含有C、H、O元素 |
如图为元素周期表中钠元素的相关信息,下列说法正确的是( )


| A、钠为非金属元素 |
| B、钠原子的实际质量为22.99 |
C、钠元素的原子结构示意图为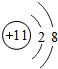 |
| D、钠原子核内质子数为11 |
在托盘天平两盘分别放置等质量的烧杯,再放入足量稀盐酸,天平仍平衡.向天平两边的烧杯分别加入下列物质后,仍保持平衡的是( )
| A、等质量的铜和氧化铜 |
| B、等质量的铁和氧化铁 |
| C、等质量的碳酸钙和碳酸钠 |
| D、等质量的铁和锌 |
 实验室需配制一定浓度的硝酸钾溶液.
实验室需配制一定浓度的硝酸钾溶液.