题目内容
8.燃烧、缓慢氧化和自燃的共同点的是( )| A. | 都发光 | B. | 都放热 | C. | 都很剧烈 | D. | 都需加热或点燃 |
分析 燃烧是指可燃物跟空气中的氧气发生的发光、发热的比较剧烈的氧化反应;有些氧化反应进行的比较缓慢,甚至不溶易被察觉,这样的氧化称为缓慢氧化;由缓慢氧化引起的自发燃烧叫自燃.它们的共同点是:都是氧化反应,都能放出热量.
解答 解:A、缓慢氧化不发光,故选项错误;
B、它们的共同点是:都是氧化反应,都能放出热量.故选项正确;
C、缓慢氧化进行的比较缓慢,故选项错误;
D、缓慢氧化和自燃就不需要加热或点燃,故选项错误;
故选B.
点评 本考点考查了燃烧、爆炸、缓慢氧化和自燃的关系,要加强记忆它们的概念,相同点和不同点,在理解和比较的基础上进行应用.本考点的基础性强,主要出现在选择题和填空题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列微粒符号中,对“2”的含义理解正确的是( )
| A. | 2Cu中的“2”表示2个铜元素 | |
| B. | Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷 | |
| C. | H2S中的“2”表示1个硫化氢分子中含 有2个硫原子 | |
| D. | S2-表示-2价的硫元素 |
19. 如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.
如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.
(1)经访问有关人员,了解到这样包装的目的是为了防止食品挤压变形或食品腐败,且从经济性、环保等因素考虑,工厂使用的包装气体是空气,氮气或二氧化碳.请你以此调查结果为依据,对包装气体的成分提出猜想,并说明你猜想的依据:
(2)请设计实验,检验上述猜想的正确性.填写下列实验报告:
(3)你认为食品充气包装,对所充气体的要求是:①无毒②与食品不反应③价廉易得.
 如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.
如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.(1)经访问有关人员,了解到这样包装的目的是为了防止食品挤压变形或食品腐败,且从经济性、环保等因素考虑,工厂使用的包装气体是空气,氮气或二氧化碳.请你以此调查结果为依据,对包装气体的成分提出猜想,并说明你猜想的依据:
| 我对气体的猜想是 | |
| 我猜想的依据是 |
| 实验方法及操作 | 可能观察到的现象及结论 |
16.下列物质中含有氧分子的是( )
| A. | 氯酸钾 | B. | 二氧化硫 | C. | 双氧水 | D. | 液氧 |
3.利用燃烧法除去空气中的氧气,得到较纯净的氮气,应选择( )
| A. | 木炭 | B. | 红磷 | C. | 铁丝 | D. | 石蜡 |
13.(1)根据指定元素或原子团的化合价填写化学式:
(2)根据化学式写出物质的名称或根据物质名称写出化学式:
①AgCl氯化银,②BaSO4硫酸钡,③FeO氧化亚铁,④ZnCl2氯化锌,
⑤硝酸镁Mg(NO3)2,⑥氧化钙CaO,⑦氢氧化铁Fe(OH)3,⑧氩气Ar,⑨碳酸钠Na2CO3.
| $\stackrel{-1}{Cl}$ | $\stackrel{-2}{O}$ | $S\stackrel{-2}{{O}_{4}}$ | |
| $\stackrel{+1}{Na}$ | |||
| $\stackrel{+2}{Ca}$ | |||
| $\stackrel{+3}{Fe}$ |
①AgCl氯化银,②BaSO4硫酸钡,③FeO氧化亚铁,④ZnCl2氯化锌,
⑤硝酸镁Mg(NO3)2,⑥氧化钙CaO,⑦氢氧化铁Fe(OH)3,⑧氩气Ar,⑨碳酸钠Na2CO3.
17.工业上常用铁质容器盛装冷浓硫酸.但铁与热浓硫酸可以发生反应.
(1)2Fe+6H2SO4(浓)═Fe2(SO4)3+mSO2↑+nH2O,则m、n的值分别为3、6.
(2)碱石灰是常用的干燥剂,实验室中不能(填“能”或“不能”)用来干燥SO2.
(3)某实验小组为研究铁质材料与热浓硫酸的反应,用铁钉(铁钉中除铁外还含有碳单质)与热浓硫酸反应,想知道反应后生成气体的成分,设计了如下探究实验:
【提出问题】反应后生成气体的成分是什么?
【查阅资料】
①碳与浓硫酸可发生反应:C+2H2SO4(浓硫酸)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O
②SO2可以使高锰酸钾和品红溶液褪色.
③无水硫酸铜遇水变蓝色.
【猜 想】
猜想1:只有SO2;猜想2:只有CO2;猜想3:可能含有H2;猜想4:含有SO2、CO2、H2(或含有SO2、CO2、不含H2,答一种情况即可).
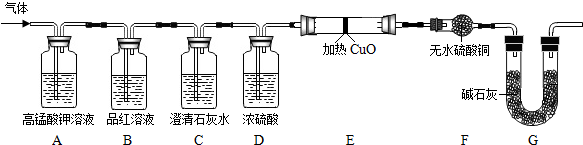
【实验探究】实验装置设计如图(其中气体为铁钉与浓硫酸反应后收集到的气体,B装置用来检验A装置反应是否完全),根据实验过程验证猜想4.

(1)2Fe+6H2SO4(浓)═Fe2(SO4)3+mSO2↑+nH2O,则m、n的值分别为3、6.
(2)碱石灰是常用的干燥剂,实验室中不能(填“能”或“不能”)用来干燥SO2.
(3)某实验小组为研究铁质材料与热浓硫酸的反应,用铁钉(铁钉中除铁外还含有碳单质)与热浓硫酸反应,想知道反应后生成气体的成分,设计了如下探究实验:
【提出问题】反应后生成气体的成分是什么?
【查阅资料】
①碳与浓硫酸可发生反应:C+2H2SO4(浓硫酸)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O
②SO2可以使高锰酸钾和品红溶液褪色.
③无水硫酸铜遇水变蓝色.
【猜 想】
猜想1:只有SO2;猜想2:只有CO2;猜想3:可能含有H2;猜想4:含有SO2、CO2、H2(或含有SO2、CO2、不含H2,答一种情况即可).
【实验探究】实验装置设计如图(其中气体为铁钉与浓硫酸反应后收集到的气体,B装置用来检验A装置反应是否完全),根据实验过程验证猜想4.
| 实验过程 | 实验现象 | 实验结论 |
| 1°气体通过高锰酸钾溶液. | 高锰酸钾溶液褪色. | 猜想4成立 |
| 2°气体通过澄清石灰水. | 澄清石灰水变浑浊. | |
| 3°气体通过氧化铜和无水硫酸铜. | 黑色氧化铜变红色,无水硫酸铜变蓝色(合理即可). |
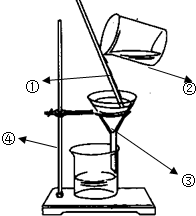 (1)指出图中所标的仪器的名称
(1)指出图中所标的仪器的名称