题目内容
16.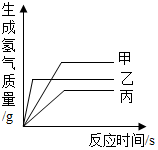 等质量的甲、乙、丙三种金属分别与等质量且溶质质量分数相等的稀硫酸充分反应,生成+2价的硫酸盐,产生氢气的质量与反应时间的关系如图,则下列说法错误的是( )
等质量的甲、乙、丙三种金属分别与等质量且溶质质量分数相等的稀硫酸充分反应,生成+2价的硫酸盐,产生氢气的质量与反应时间的关系如图,则下列说法错误的是( )| A. | 三种金属的活动性大小为乙>甲>丙 | |
| B. | 反应时消耗硫酸的质量一定相同 | |
| C. | 三种金属的相对原子质量是丙>乙>甲 | |
| D. | 反应结束时,丙一定没有剩余 |
分析 据相同时间内产生氢气较多(即反应剧烈)的金属活动性较强,结合产生氢气的关系图判断三种金属活动性;
根据一定质量的金属完全反应产生氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}$×金属的质量,结合三种金属的化合价及完全反应放出氢气的质量大小,判断三种金属的相对原子质量的大小.
解答 解:A、根据反应生成H2的质量与反应时间的关系图所示,当三种金属都在发生反应时,相同时间内乙放出氢气的质量大于甲、大于丙,可判断三种金属活动性顺序是乙>甲>丙,正确;
B、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗硫酸的质量:甲>乙>丙,错误;
C、三种金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是甲>乙>丙;因此可判断相对原子质量是丙>乙>甲,正确;
D、根据反应生成H2的质量与反应时间的关系图所示,反应结束时,丙一定没有剩余,正确;
故选B
点评 对于活泼金属,活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比.

练习册系列答案
相关题目
6.下列实验描述不正确的是( )
| A. | 夜间若发现煤气泄漏,应立即开灯检查 | |
| B. | 可用燃着的木条来检验二氧化碳是否收集已满 | |
| C. | 实验之室制备气时,装药品前应先检查装置的气密性 | |
| D. | 电解水实验中,与电源负极相连的玻璃管内产生的气体能燃烧 |
4.下列说法正确的组合是( )
①空气是一种宝贵的自然资源;
②所谓“低碳”就是较低的二氧化碳排放;
③爱护水资源一方面要节约用水,另一方面要防治水体污染;
④利用碳的还原性冶炼金属.
①空气是一种宝贵的自然资源;
②所谓“低碳”就是较低的二氧化碳排放;
③爱护水资源一方面要节约用水,另一方面要防治水体污染;
④利用碳的还原性冶炼金属.
| A. | ①②③ | B. | ①③④ | C. | ①②③④ | D. | ②③④ |
11.下列有关水的说法不正确的是( )
| A. | 我国淡水资源是取之不尽,用之不竭的 | |
| B. | 氢气在氧气燃烧生成水也能说明水是由氢、氧两种元素组成 | |
| C. | 海水、湖水是混合物,蒸馏水是纯净物 | |
| D. | 生活中用煮沸的方法使硬水软化 |
8.下列实验现象描述正确的是( )
| A. | 木炭在氧气中燃烧,发出白光,放出热量 | |
| B. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| C. | 打开浓盐酸瓶盖有白烟 | |
| D. | 向稀硫酸溶液中滴入紫色石蕊溶液,溶液变成蓝色 |
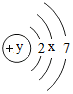 ,x=8,其中y=17.
,x=8,其中y=17.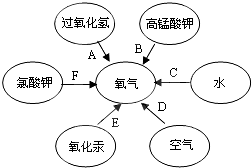 我们学过有六种途径可制得氧气,如图所示:
我们学过有六种途径可制得氧气,如图所示: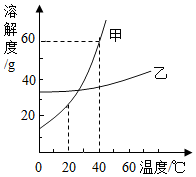 如图所示:40℃时,甲的饱和溶液中溶质:溶剂和溶液的质量比为:3:5:8,甲物质易溶(填难或微或易)
如图所示:40℃时,甲的饱和溶液中溶质:溶剂和溶液的质量比为:3:5:8,甲物质易溶(填难或微或易)