题目内容
18. 在公共场所有如图广告,请回答下列问题:
在公共场所有如图广告,请回答下列问题:纯碳酸氢铵(NH4HCO3)中氮元素的质量分数是17.7%,该化肥的纯度(即化肥中NH4HCO3的质量分数)因故缺损了,请你补上:96.0%(计算结果小数点后保留一位小数).
施用注意事项:避免雨天、高温天气施用,不要与碱性物质混用.由此可推测碳酸氢铵的性质有:
物理性质:白色固体,易溶于水.
化学性质:热稳定性差,能和碱性物质反应.
分析 根据碳酸氢铵(NH4HCO3)中氮元素的质量分数为:$\frac{原子的相对原子质量×原子个数}{相对分子质量}$×100%;根据质量分数公式,化肥中的含氮量÷纯碳酸氢铵的含氮量=该化肥的纯度.可以根据具体的描述进行分析、判断,从而得出正确的结论.
解答 解:碳酸氢铵(NH4HCO3)中氮元素的质量分数=$\frac{14}{14+1×5+12+16×3}×$100%≈17.7%;
该化肥的纯度为:17%÷17.7%≈96.0%;
碳酸氢铵的物理性质有:白色固体,易溶于水.
受热易分解属于物质的化学性质,能和显碱性的物质反应属于物质的化学性质,所以化学性质有:热稳定性差,能和碱性物质反应.
答案:17.7%;96.0%;白色固体,易溶于水;热稳定性差,能和碱性物质反应.
点评 本题主要考查学生运用化学式和元素的质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
9.下列有关说法,正确的是( )
| A. | 干燥的空气中体积分数含量最多的是氧气 | |
| B. | 氧气的化学性质比较活泼,可以与任何物质发生反应 | |
| C. | 工业上根据氮气和氧气的沸点不同,采取分离液态空气法制取氧气 | |
| D. | 加热高锰酸钾制取氧气反应完毕后,试管内剩余的固体属于纯净物 |
6.下列物质不是分子构成的是( )
| A. | 氧气 | B. | 铁 | C. | 氨气 | D. | 氯化氢 |
3.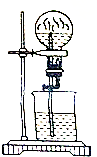 在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶,则a和b分别是( )
在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶,则a和b分别是( )
 在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶,则a和b分别是( )
在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶,则a和b分别是( ) | a(干燥气体) | b(液体) | |
| A | N2 | 水 |
| B | O2 | 饱和NaCl溶液 |
| C | H2 | 稀盐酸 |
| D | CO2 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
6.下列关于实验现象的描述正确的是( )
| A. | 红热的铁丝伸入空气中,剧烈燃烧,火星四射,生成黑色固体 | |
| B. | 水通电后生成氢气和氧气 | |
| C. | 打开浓盐酸的试剂瓶,瓶口有白雾 | |
| D. | 将硝酸钾溶液和氯化钡溶液混合,产生白色沉淀 |