题目内容
6.结合下列装置图回答问题: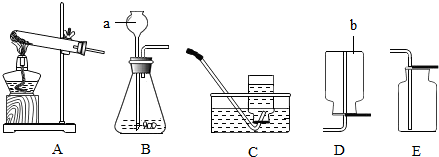
(1)写出如图中有标号仪器的名称:a.长颈漏斗;b.集气瓶.
(2)实验室制取和收集CO2气体时,应选用BE (填序号),化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.检验生成的二氧化碳气体,相应的反应方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
(3)氨气是一种无色有刺激性气味,极易溶于水,密度比空气小的气体.某学习小组在探究活动中要制取一定量的氨气,采用氯化铵固体和熟石灰粉末在加热条件下生成氨气.
请问:制取氨气的装置是A (填序号,下同);收集氨气的装置是D.
分析 (1)熟记仪器的名称;
(2)用碳酸钙和稀盐酸制取H2,是固体与液体在常温下反应,要采用B作发生装置;二氧化碳能溶于水,密度大于空气,故选择E作收集装置;实验室用澄清的石灰水来检验二氧化碳气体;
(3)根据氯化铵固体和熟石灰粉末在加热条件下生成氨气,选取发生装置;依据氨气是一种无色有刺激性气味、极易溶于水、密度比空气小的气体,选取收集装置.
解答 解;(1)a是长颈漏斗;b是集气瓶.故填:长颈漏斗;集气瓶;
(2)用碳酸钙和稀盐酸制取二氧化碳,是固体与液体在常温下反应,要采用B作发生装置,实验室制取二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳能溶于水,密度大于空气,故选择E作收集装置,检验CO2气体的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O;
故填:BE;CaCO3+2HCl=CaCl2+H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O
(3)根据氯化铵固体和熟石灰粉末在加热条件下生成氨气,选取发生装置为A;依据氨气是一种无色有刺激性气味、极易溶于水、密度比空气小的气体,选取收集装置为D;故填:A;D.
点评 本题考查学生对常用气体的发生装置和收集装置与选取方法及其依据的理解,根据气体的制取原理来组装、选配、判断或者选择气体的发生装置;再根据气体的溶解性、密度及其是否与水或者空气发生反应等来判断、选用收集装置.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
1.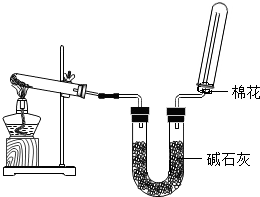 如图是制取氨气的装置图,原料为熟石灰和氯化铵固体.下列说法正确的是( )
如图是制取氨气的装置图,原料为熟石灰和氯化铵固体.下列说法正确的是( )
 如图是制取氨气的装置图,原料为熟石灰和氯化铵固体.下列说法正确的是( )
如图是制取氨气的装置图,原料为熟石灰和氯化铵固体.下列说法正确的是( )| A. | 直接给试管加热,不必进行预热 | |
| B. | 氨气的密度比空气大 | |
| C. | 将一湿润的蓝色石蕊试纸放在试管口,若变红,证明已满 | |
| D. | 铵态氮肥不能与碱性物质混合使用,以防氮肥损失 |
 生命吸管是能够将河水、泉水等直接过滤成直饮水的便携式净水装备.
生命吸管是能够将河水、泉水等直接过滤成直饮水的便携式净水装备.
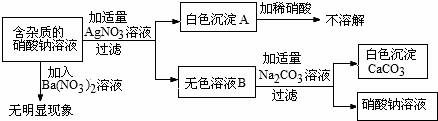
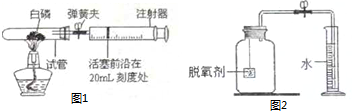 我校化学兴趣小组测定空气中氧气的含量,并改进教材方案.
我校化学兴趣小组测定空气中氧气的含量,并改进教材方案.