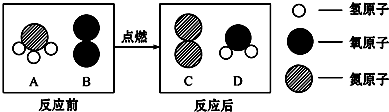
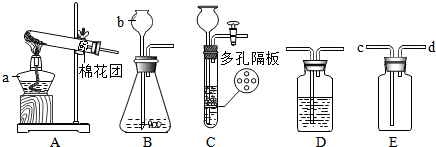
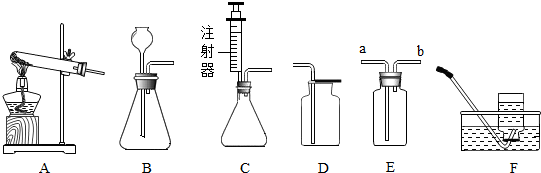
��Ŀ����
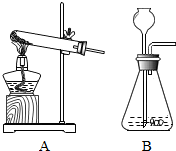 �ع�ʵ������ȡO2��ʵ�飬���ǿ�֪���о�ʵ������ȡ�����һ��˳��
�ع�ʵ������ȡO2��ʵ�飬���ǿ�֪���о�ʵ������ȡ�����һ��˳����1�������о����ɸ�����Ļ�ѧ��Ӧԭ����
��2��Ȼ����ݷ�Ӧ���״̬�ͷ�Ӧ������ѡ��װʵ������������һ��Ҫ���
��3�������ռ������
��4��ͼ����������������װ�ã���Ҫ��ش�
�ټ�������غͶ������̻������ȡ�����Ļ�ѧ����ʽΪ
��ʵ�����ù�������Ͷ���������������ѡ
��ij��ȤС��ȡ120�˹���������Һ��3�˶������̵������·�Ӧ����Ӧһ��ʱ�����������ʣ�����ʵ�������Ϊ119.8�ˣ��Լ��㣺
��A����ʵ������������������Ϊ
��B�����ݻ�ѧ����ʽ��ʽ����μӷ�Ӧ�Ĺ�����������ʵ�����
�����⣨H2S����һ�־��г�������ζ�����壬���ܶȱȿ������ܶȴ���������ˮ�γ������ᣮʵ����ͨ���ÿ�״������������FeS����ϡ���ᣨH2SO4����ϣ��ڳ����·�����Ӧ���������������������壮�Իش�
��A��ʵ������ȡ����Ļ�ѧ��Ӧ����ʽΪ��
��B����ȡ��������ķ���װ�ÿ���ѡ��
��C���ռ������������
���㣺��������ȡװ��,�����ķ��뷽��,ʵ������ȡ�����˼·,�������ռ�����,��д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ,���ݻ�ѧ��Ӧ����ʽ�ļ���
ר�⣺���������ʵ�����Ʒ������顢�����뾻��
��������2������������μӻ������ʵ�飬ʵ��ǰһ��Ҫ���װ�õ������ԣ��Է�װ��©��Ӱ��ʵ������
��3��������ȡ����ķ�Ӧ��״̬����Ӧ��������������ʿ���ѡ����װ�ú��ռ�װ��
��4��������ڶ������̵Ĵ������£����ȷֽ������Ȼ��غ�������
���˿��Ѳ�����ˮ�����ʳ�ȥ���������Եõ����壻
���ʵ���=
��
��3��������ȡ����ķ�Ӧ��״̬����Ӧ��������������ʿ���ѡ����װ�ú��ռ�װ��
��4��������ڶ������̵Ĵ������£����ȷֽ������Ȼ��غ�������
���˿��Ѳ�����ˮ�����ʳ�ȥ���������Եõ����壻
���ʵ���=
| ���ʵ����� |
| ���ʵ�Ħ������ |
����⣺��2�����ݷ�Ӧ���״̬�ͷ�Ӧ������ѡ��װʵ������������һ��Ҫ���װ�õ������ԣ�
���װ�õ������ԣ�
��3�������ռ�������ܶȺ�ˮ����ȷ��������ռ�������
����ܶȣ�ˮ���ԣ�
��4���ټ�������غͶ������̻������ȡ�����Ļ�ѧ����ʽΪ��2KClO3
2KCl+3O2����
����ʱ���Ƚ����������ձ��У�������ˮ�����裻
�����õ�����Һ���й��ˣ��ɵõ��������̣�
����Һ�����������ɵõ��Ȼ��أ�
���2KClO3
2KCl+3O2����ˮ�����裻���ˣ��������̣��������Ȼ��أ�
��ʵ�����ù�������Ͷ���������������ѡBװ�ã�ԭ���Ƿ�Ӧ����Һ����壬����Ҫ���ȣ�
���B����Ӧ����Һ����壬����Ҫ���ȣ�
�ۣ�A����ʵ������������������Ϊ��120g+3g-119.8g=3.2g��
���������ʵ���Ϊ��
=0.1mol��
���3.2��0.1��
��B����������������Ϊx��
2H2O2
2H2O+O2����
68 32
x 3.2g
=
��
x=6.8g��
�𣺲μӷ�Ӧ�Ĺ�������������6.8g��
�ܣ�A��ʵ������ȡ����Ļ�ѧ��Ӧ����ʽΪ��FeS+H2SO4�TFeSO4+H2S����
��B����Ϊ��Ӧ����Ҫ���ȣ���ȡ��������ķ���װ�ÿ���ѡ��Bװ�ã�
��C����Ϊ�����ܹ�����ˮ����������ˮ���ռ����ܶȱȿ������ռ�����������������ſ�������
���FeS+H2SO4�TFeSO4+H2S����B�������ſ�����
���װ�õ������ԣ�
��3�������ռ�������ܶȺ�ˮ����ȷ��������ռ�������
����ܶȣ�ˮ���ԣ�
��4���ټ�������غͶ������̻������ȡ�����Ļ�ѧ����ʽΪ��2KClO3
| ||
| �� |
����ʱ���Ƚ����������ձ��У�������ˮ�����裻
�����õ�����Һ���й��ˣ��ɵõ��������̣�
����Һ�����������ɵõ��Ȼ��أ�
���2KClO3
| ||
| �� |
��ʵ�����ù�������Ͷ���������������ѡBװ�ã�ԭ���Ƿ�Ӧ����Һ����壬����Ҫ���ȣ�
���B����Ӧ����Һ����壬����Ҫ���ȣ�
�ۣ�A����ʵ������������������Ϊ��120g+3g-119.8g=3.2g��
���������ʵ���Ϊ��
| 3.2g |
| 32g/mol |
���3.2��0.1��
��B����������������Ϊx��
2H2O2
| ||
68 32
x 3.2g
| 68 |
| x |
| 32 |
| 3.2g |
x=6.8g��
�𣺲μӷ�Ӧ�Ĺ�������������6.8g��
�ܣ�A��ʵ������ȡ����Ļ�ѧ��Ӧ����ʽΪ��FeS+H2SO4�TFeSO4+H2S����
��B����Ϊ��Ӧ����Ҫ���ȣ���ȡ��������ķ���װ�ÿ���ѡ��Bװ�ã�
��C����Ϊ�����ܹ�����ˮ����������ˮ���ռ����ܶȱȿ������ռ�����������������ſ�������
���FeS+H2SO4�TFeSO4+H2S����B�������ſ�����
������������Ҫ����Ӧ����ʽ����д��ʵ��װ�õ�ѡ��ѡ����װ��ʱ��Ҫ���Ƿ�Ӧ���״̬����Ӧ���������أ�ѡ���ռ�װ��ʱ��Ҫ���������ˮ���ԡ��ܷ��ˮ������ѧ��Ӧ���ܶȡ��ܷ�Ϳ����е����ʷ�����ѧ��Ӧ�����أ�

��ϰ��ϵ�д�
 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
�����Ŀ
���и�����Һ�����������Լ����ܼ�����ǣ�������
| A��NaOH��NaCl��MgCl2��FeCl3 |
| B��Na2CO3��ϡH2SO4��ϡHCl��NaNO3 |
| C��Na2SO4��BaCl2��KNO3��NaCl |
| D��K2SO4��Na2CO3��BaCl2��NaNO3 |
ʵ�����ù�������Ͷ������̻����ȡ����ʱ���������̵������ǣ�������
| A�������������� |
| B���ӿ��������ķֽ��ٶ� |
| C���������� |
| D���ȼӿ��������ķֽ��ٶȣ��������������� |
����˵����ȷ���ǣ�������
| A������Ԫ��������������� |
| B�������ǻ�ѧ�仯�е���С���� |
| C��ԭ�Ӳ������ٷ� |
| D�����ӡ�ԭ�ӡ����Ӷ�����ֱ�ӹ������� |
����ʵ������У���ȷ���ǣ�������
A��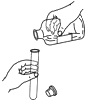 �㵹Һ�� |
B��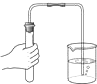 ��������� |
C��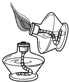 ��ȼ�ƾ��� |
D��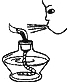 Ϩ��ƾ��� |