题目内容
2.根据下列装置,回答有关问题: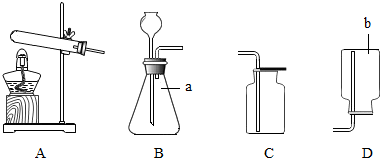
(1)写出装置图中标号仪器的名称a锥形瓶,b集气瓶.
(2)写出实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,可选用的收集装置是C(填字母).
(3)写出实验室用石灰石与稀盐酸反应制取二氧化碳的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑,可选用的发生装置是B(填字母).
(4)实验室将A装置加以改动,在高温下是碳酸钙分解生成氧化钙和二氧化碳,按此反应,试计算工业上要制取5.6t氧化钙,理论上需要含碳酸钙80%的石灰石的质量是多少?
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据过氧化氢在二氧化锰的催化作用下生成水和氧气,氧气密度比空气大进行分析;
(3)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,该反应的反应物是固体,反应条件是常温进行分析;
(4)根据碳酸钙在高温的条件下生成氧化钙和二氧化碳,然后结合氧化钙的质量计算碳酸钙的质量.
解答 解:(1)通过分析题中所指仪器的仪器的作用可知,a是锥形瓶,b是集气瓶;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,氧气密度比空气大,可选用的收集装置是C;
(3)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应的反应物是固体,反应条件是常温,可选用的发生装置是B;
(4)设理论上需要碳酸钙的质量为x,
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56
x 5.6t
$\frac{100}{x}$=$\frac{56}{5.6t}$
x=10t,
含碳酸钙80%的石灰石的质量为:10t÷80%=12.5t.
故答案为:(1)锥形瓶,集气瓶;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,C;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑,B;
(4)12.5t.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
相关题目
12.如表是固体甲和乙在不同温度时的溶解度.下列说法中正确的是( )
| 温度/℃ | 0 | 20 | 40 | 100 |
| 甲溶解度/克 | 0.173 | 0.165 | 0.121 | 0.076 |
| 乙溶解度/克 | 13.3 | 31.6 | 63.9 | 246 |
| A. | 20℃时甲物质的饱和溶液升高温度会变为不饱和溶液 | |
| B. | 100℃时乙物质的饱和溶液冷却到室温会析出晶体,但溶液仍饱和 | |
| C. | 20℃时.甲溶液的溶质质量分数一定小于乙溶液的溶质质量分数 | |
| D. | 20℃时,100克乙物质加入100克水中.所得溶液的溶质质量分数等于50% |
10.下列物质不是人体所需营养素的是( )
| A. | 尼古丁 | B. | 水 | C. | 蛋白质 | D. | 维生素 |
17.用灯帽盖灭酒精灯,其主要灭火原理是( )
| A. | 隔绝空气 | B. | 清除可燃物 | ||
| C. | 降低酒精灯的着火点 | D. | 使温度降到酒精的着火点以下 |
16.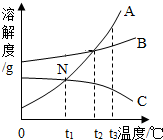 如图是ABC三种物质的溶解度曲线,下列说法正确的是( )
如图是ABC三种物质的溶解度曲线,下列说法正确的是( )
 如图是ABC三种物质的溶解度曲线,下列说法正确的是( )
如图是ABC三种物质的溶解度曲线,下列说法正确的是( )| A. | 三种物质中A的溶解度最大 | |
| B. | AB两种物质的饱和溶液从t3降温到t1,A析出的晶体多 | |
| C. | ABC三种物质的饱和溶液从t3降温到t1,所得溶液的溶质质量分数B=C>A | |
| D. | 升高温度C的不饱和溶液可以变为饱和溶液 |
17.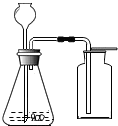 使用如图装置可以进行下列实验中的( )
使用如图装置可以进行下列实验中的( )
 使用如图装置可以进行下列实验中的( )
使用如图装置可以进行下列实验中的( )| A. | 锌与稀硫酸制取、收集氢气 | |
| B. | 加热氯酸钾与二氧化锰制取、收集氧气 | |
| C. | 加热高锰酸钾制取、收集氧气 | |
| D. | 过氧化氢溶液与二氧化锰制取、收集氧气 |
 1879年10月,经过对1600多种材料进行几千次试验后,爱迪生制成了第一个可供实用的碳丝灯泡(灯丝由竹丝炭化后制成).
1879年10月,经过对1600多种材料进行几千次试验后,爱迪生制成了第一个可供实用的碳丝灯泡(灯丝由竹丝炭化后制成). 通过近一年的化学学习,你已经掌握了实验室制取气体的有关方法.请根据图回答问题:
通过近一年的化学学习,你已经掌握了实验室制取气体的有关方法.请根据图回答问题: