题目内容
在学习碱的化学性质时,李老师给同学们演示了下面的三个实验:
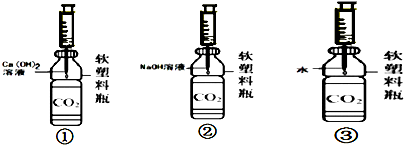
相同温度下,有三个同样的装满二氧化碳的软塑料瓶,在①②号瓶中分别滴加等质量的饱和氢氧化钙溶液和饱和氢氧化钠溶液,在③号瓶中滴加等质量的水.充分振荡后,观察现象.
(1)写出三个软塑料瓶中产生相同现象的原因: ;
(2)写出①②号两个软塑料瓶中产生的不同现象是 ;
(3)对比①②瓶中现象你能得到怎样的结论: ;
(4)实验②③进行对比的目的是要验证氢氧化钠的什么化学性质(用化学方程式表示): .

相同温度下,有三个同样的装满二氧化碳的软塑料瓶,在①②号瓶中分别滴加等质量的饱和氢氧化钙溶液和饱和氢氧化钠溶液,在③号瓶中滴加等质量的水.充分振荡后,观察现象.
(1)写出三个软塑料瓶中产生相同现象的原因:
(2)写出①②号两个软塑料瓶中产生的不同现象是
(3)对比①②瓶中现象你能得到怎样的结论:
(4)实验②③进行对比的目的是要验证氢氧化钠的什么化学性质(用化学方程式表示):
考点:碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:(1)根据二氧化碳的性质分析判断;
(2)根据二氧化碳和氢氧化钙的反应、二氧化碳和氢氧化钠反应的现象、氢氧化钙、氢氧化钠在水中溶解性判断;
(3)根据二氧化碳和氢氧化钙的反应、二氧化碳和氢氧化钠反应的现象解答;
(4)
(2)根据二氧化碳和氢氧化钙的反应、二氧化碳和氢氧化钠反应的现象、氢氧化钙、氢氧化钠在水中溶解性判断;
(3)根据二氧化碳和氢氧化钙的反应、二氧化碳和氢氧化钠反应的现象解答;
(4)
解答:解:(1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,二氧化碳和氢氧化钠反应生成碳酸钠和水、二氧化碳和水反应生成碳酸,所以三瓶内气压都减小,瓶子变瘪,故答案:三种物质都能与二氧化碳反应,且不生成新的气体,使瓶内气体减少,气压减小,小于外压,压强差的作用下,瓶子都变瘪.
(2)二氧化碳和澄清石灰水反应产生白色沉淀,二氧化碳和氢氧化钠反应生成碳酸钠和水,但无明显现象,但氢氧化钙微溶于水,氢氧化钠溶于水,所以②号瓶子吸收的二氧化碳更多,气压减小更大,瓶子变瘪程度更明显,故答案:①号溶液中产生白色浑浊,②号溶液无明显变化;②号瓶子变瘪程度比①号瓶大;
(3)二氧化碳和澄清石灰水反应产生白色沉淀,二氧化碳和氢氧化钠反应生成碳酸钠和水,但氢氧化钙微溶于水,氢氧化钠溶于水,所以②号瓶子吸收的二氧化碳更多,故答案:鉴别二氧化碳用氢氧化钙溶液,吸收二氧化碳用氢氧化钠溶液;
(4)二氧化碳和水反应生成碳酸,碳酸和氢氧化钠反应生成碳酸钠和水,反应的化学方程式为CO2+H2O=H2CO3;H2CO3+2NaOH=Na2CO3+2H2O,故答案:CO2+H2O=H2CO3;H2CO3+2NaOH=Na2CO3+2H2O.
(2)二氧化碳和澄清石灰水反应产生白色沉淀,二氧化碳和氢氧化钠反应生成碳酸钠和水,但无明显现象,但氢氧化钙微溶于水,氢氧化钠溶于水,所以②号瓶子吸收的二氧化碳更多,气压减小更大,瓶子变瘪程度更明显,故答案:①号溶液中产生白色浑浊,②号溶液无明显变化;②号瓶子变瘪程度比①号瓶大;
(3)二氧化碳和澄清石灰水反应产生白色沉淀,二氧化碳和氢氧化钠反应生成碳酸钠和水,但氢氧化钙微溶于水,氢氧化钠溶于水,所以②号瓶子吸收的二氧化碳更多,故答案:鉴别二氧化碳用氢氧化钙溶液,吸收二氧化碳用氢氧化钠溶液;
(4)二氧化碳和水反应生成碳酸,碳酸和氢氧化钠反应生成碳酸钠和水,反应的化学方程式为CO2+H2O=H2CO3;H2CO3+2NaOH=Na2CO3+2H2O,故答案:CO2+H2O=H2CO3;H2CO3+2NaOH=Na2CO3+2H2O.
点评:澄清石灰水通入二氧化碳变浑浊,实验室通常利用这一变化检验气体是不是二氧化碳.二氧化碳和氢氧化钠反应生成碳酸钠和水,氢氧化钠可用于吸收二氧化碳.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
下列变化属于化学变化的是( )
| A、浓盐酸挥发 |
| B、氢氧化钠潮解 |
| C、浓硫酸腐蚀衣服 |
| D、电灯发光 |
氧气的化学性质比较活泼,能与多种物质反应.下列对有关反应的描述正确的是( )
| A、在点燃的条件下,硫在氧气里燃烧,发出蓝紫色火焰,生成无色无味的气体 |
| B、在点燃的条件下,细铁丝在氧气中剧烈燃烧,火星四射,生成黑色的三氧化二铁 |
| C、铁、硫、酒精在氧气中的燃烧都是化合反应 |
| D、物质与氧气发生的反应属于氧化反应,氧气具有氧化性 |
下列图示不属于模型的是( )
A、 足球烯 |
B、 眼球 |
C、 地球仪 |
D、 北京奥运 |
某元素的相对原子质量为264,质子数88,它的中子数为( )
| A、88 | B、264 |
| C、352 | D、176 |