题目内容
15.高铁的建成使从郑州到各地的旅行更加方便、快捷.(1)高铁列车车体用铝合金材料而不用纯铝的原因是什么?
(2)铺设铁轨需要大量的钢铁,写出高炉炼铁发生反应的化学方程式.
分析 (1)根据铝合金、纯铝的性能比较分析;
(2)根据工业炼铁是一氧化碳和氧化铁反应生成铁和二氧化碳进行分析.
解答 解:(1)合金与纯金属相比,具有硬度大、熔点低、耐腐蚀性能好等特点.而使用铝合金,除了以上优点外,还有密度小的优势,可以减少动车的能量消耗.因此,高铁列车车体用铝合金材料而不用纯铝的原因是铝合金硬度大,抗腐蚀性能好于纯铝.
(2)工业炼铁是一氧化碳和氧化铁反应生成铁和二氧化碳,故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故答案为:(1)铝合金硬度大,抗腐蚀性能好于纯铝;(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 化学来源于生产、生活,也服务于生产、生活.学以致用,能用所学知识解释和处理身边的现象,这才是学习的目的和教育的本质.

练习册系列答案
相关题目
5.小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$ Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
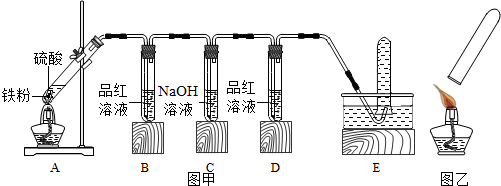
请帮助小明完成如表:
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫.
【交流反思】(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置中反应的化学方程式:2NaOH+SO2=Na2SO3+H2O.
【拓展延伸】在初中化学教材中也有反应物浓度不同,生成的产物不同的例子碳在氧气充足时生成二氧化碳不充足时生成一氧化碳.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$ Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.

请帮助小明完成如表:
| A中硫 酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品 红溶液 | D中品 红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有二氧化硫和氢气 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
【交流反思】(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置中反应的化学方程式:2NaOH+SO2=Na2SO3+H2O.
【拓展延伸】在初中化学教材中也有反应物浓度不同,生成的产物不同的例子碳在氧气充足时生成二氧化碳不充足时生成一氧化碳.
3.小红在餐厅看到服务员用盖子熄灭燃着的固体酒精,该灭火方法的主要原理是( )
| A. | 使可燃物的温度降低到着火点以下 | B. | 隔绝氧气 | ||
| C. | 降低可燃物的着火点 | D. | 移走可燃物 |
7.有X、Y、Z三种金属,只有Z在自然界中主要以单质形式存在,如果把Y加入X的硝酸盐溶液中,Y表面有X析出,则这三种金属的活动性由强到弱的顺序为( )
| A. | Y>Z>X | B. | Y>X>Z | C. | X>Y>Z | D. | Z>Y>X |
5.如图是某粒子的结构示意图,下列说法正确的是( )


| A. | 若X=12,该粒子和氧离子形成物质的化学式是XCl | |
| B. | 若该粒子属于原子,则一定有两个电子层 | |
| C. | X元素在形成化合物时,X元素一定显负价 | |
| D. | 该粒子属于不稳定结构 |
 水是生命之源,人类的生产、生活离不开水.
水是生命之源,人类的生产、生活离不开水. 春季人的肝火会比较旺,菠菜为春天应时蔬菜,是含铁量最高的蔬菜,具有滋阴润燥、舒肝养血等作用,对春季因肝阴不足所致的高血压、贫血等都有较好的辅助治疗作用.请填写下列空白:
春季人的肝火会比较旺,菠菜为春天应时蔬菜,是含铁量最高的蔬菜,具有滋阴润燥、舒肝养血等作用,对春季因肝阴不足所致的高血压、贫血等都有较好的辅助治疗作用.请填写下列空白: