题目内容
16.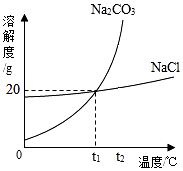 我国化学家侯德榜创立的候氏制碱法,是以海水“晒盐”得到的氯化钠为原料.制得纯碱(Na2CO3).Na2CO3和NaCl的溶解度曲线(如图所示)试回答下列问题:
我国化学家侯德榜创立的候氏制碱法,是以海水“晒盐”得到的氯化钠为原料.制得纯碱(Na2CO3).Na2CO3和NaCl的溶解度曲线(如图所示)试回答下列问题:(1)t1℃时,Na2CO3的溶解度等于NaCl的溶解度(填“大于”“等于”“小于”之一);
(2)写出一条P点表示的意义在t1℃时,Na2CO3和NaCl的溶解度相等;
(3)若Na2CO3中混有少量的NaCl固体,可用降温结晶方法提纯Na2CO3;
(4)t1℃时,将15gNa2CO3固体加入到50g水中,充分溶解后,所得溶液的溶质质量分数为16.7%(精确至0.1%).
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,t1℃时,Na2CO3的溶解度等于NaCl的溶解度;
(2)在t1℃时,Na2CO3和 NaCl的溶解度相等;
(3)碳酸钠的溶解度受温度影响变化较大,所以若Na2CO3中混有少量的NaCl固体,可用降温结晶方法提纯Na2CO3;
(4)t1℃时,碳酸钠的溶解度是20g,所以将15gNa2CO3固体加入到50g水中,充分溶解后,所得溶液的溶质质量分数为:$\frac{10g}{10g+50g}$×100%=16.7%.
故答案为:(1)等于;
(2)在t1℃时,Na2CO3和 NaCl的溶解度相等(或在t2℃时Na2CO3和 NaCl饱和溶液的溶质质量分数相等);
(3)降温结晶(或冷却热饱和溶液);
(4)16.7%.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.如图是对四个实验绘制的图象,其中实验结果与图象正确的是( )
| A. | 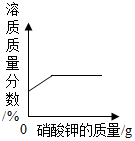 某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体 | |
| B. | 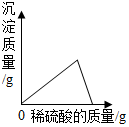 将稀硫酸滴入一定量的BaCl2溶液中 | |
| C. | 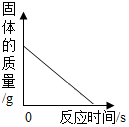 将一定质羹的石灰石加入试管中充分高温煅烧 | |
| D. | 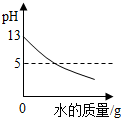 向pH为13的NaOH溶液中加水稀释 |
7.一种物质在氧气中燃烧,生成物中只有水和二氧化碳,则此物质是( )
| A. | 一定含碳氧两种元素 | B. | 一定含碳氢两种元素 | ||
| C. | 一定含碳氢氧三种元素 | D. | 不能确定 |
11.有三瓶失去标签的无色溶液,只知道它们分别是NaOH、NaCl、BaCl2中的各一种.下列四种溶液中,能将三种无色溶液一次鉴别出来的是( )
| A. | 硫酸铜溶液 | B. | 酚酞试液 | C. | 硝酸银溶液 | D. | 稀硫酸 |
1.下列结论或解释中不正确的是( )
| A. | 临泉县桃花岛桃花开放时埋怨飘香--说明分子在不断运动 | |
| B. | 水烧开后易把壶盖冲起--说明温度升高分子体积会变大 | |
| C. | 金刚石和石墨的物理性质相差较大--构成它们的碳原子的排列方式不同 | |
| D. | 水和过氧化氢化学性质不同是因为分子构成不同 |
6.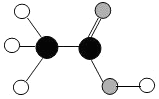 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 代表一个碳原子,
代表一个碳原子, 代表一个氢原子,
代表一个氢原子, 代表一个氧原子.下列说法正确的是( )
代表一个氧原子.下列说法正确的是( )
 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 代表一个碳原子,
代表一个碳原子, 代表一个氢原子,
代表一个氢原子, 代表一个氧原子.下列说法正确的是( )
代表一个氧原子.下列说法正确的是( )| A. | 乙酸是一种化合物 | |
| B. | 乙酸的相对分子质量为60 | |
| C. | 乙酸中碳元素的质量分数最大 | |
| D. | 乙酸分子中的碳原子、氢原子、氧原子的个数比为1:2:1 |
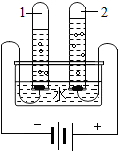 水是一种重要的资源.
水是一种重要的资源.