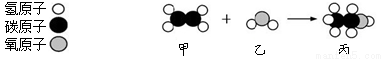
题目内容
(7分)某化学课外活动小组在整理化学试剂时,发现一瓶标签残缺的无色液体(如图所示)。

他们对此瓶无色液体是什么产生了兴趣,于是进行了如下探究。
【猜想与假设】
猜想一:硫酸铜溶液
猜想二:稀硫酸溶液
猜想三:过氧化氢溶液
小组同学对标签又进行了仔细的观察分析,他们一致认为猜想一不合理。理由是 。
【设计方案】
同学们结合所学知识设计出如下方案:
向盛有少量二氧化锰的试管中加入适量的该液体,并将带火星的木条放在试管口。
【实验与事实】
按上述方案进行实验, 发现有大量气泡产生,带火星的木条复燃。
发现有大量气泡产生,带火星的木条复燃。
【结论与解释】
(1)以上事实证明猜想 是正确的。
(2)产生气体的反应可以用化学方程式表示为
【反思与评价】
(1)在实验中,某同学提出应该先将气体收集,然后用带火星的木条检验,你认为 (选填“有”或“没有”)必要。
(2)为避免在今后的实验中出现标签残缺的情况,在倾倒液体时应注意
【拓展与迁移】
根据探究结果,重新贴好标签。标签上化学式中氧元素的化合价为 。(氢元素显+1价)
硫酸铜溶液是蓝色或硫酸铜中无氢元素; 三 ; 2H2O2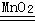 2H2O+O2↑ ; 没有 ; 标签面向手心 ; -1
2H2O+O2↑ ; 没有 ; 标签面向手心 ; -1
【解析】
试题分析:【猜想与假设】硫酸铜溶液为蓝色;【设计方案】(1)根据实验现象可知,猜想三正确;(2)化学方程式为:2H2O2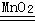 2H2O+O2↑;【反思与评价】(1)没有必要收集后再检验;(2)倾倒液体时标签要向着手心;化学式为H2O2,假设氧元素化合价为X ,(+1)*2+2x=0 x=-1。
2H2O+O2↑;【反思与评价】(1)没有必要收集后再检验;(2)倾倒液体时标签要向着手心;化学式为H2O2,假设氧元素化合价为X ,(+1)*2+2x=0 x=-1。
考点:实验方案的收集与评价。

练习册系列答案
相关题目