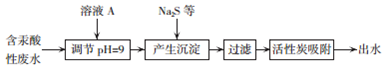
题目内容
11.如图1所示的仪器和装置,可用于实验室制取氧气,请回答有关问题: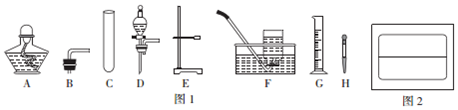
(1)实验室用加热氯酸钾和二氧化锰的方法来制取氧气,反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.组装发生装置时需选择如图1中的仪器有ABCE(填字母序号);若完成硫粉在氧气中燃烧的实验,最好选用如图1中的F装置来收集氧气,理由是集气瓶底部可留少量水,用于吸收硫燃烧生成的二氧化硫,防止其污染空气.
(2)实验室欲用5%的双氧水溶液来制取氧气,现要配制100g溶质质量分数为6%的双氧水溶液,需要20%的双氧水溶液30g,需要加入水的体积为70ml.
(3)在量取水的操作中,当水面接近所需刻度时,应该用图1中的H(填字母序号)加水至所需刻度,将配制好的溶液装入细口瓶中,贴好标签,请在如图2所示的标签内填入试剂瓶所要贴的标签内容.
分析 (1)根据氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气进行分析;根据氯酸钾制取氧气的反应物是固体,反应条件是加热进行分析;根据硫燃烧的产物二氧化硫的性质选择收集方法;
(2)根据稀释前后溶质的质量不变通过计算去分析解答;
(3)根据滴加少量的液体用胶头滴管;标签中的内容为溶液的名称及其质量分数去分析解答.
解答 解:(1)氯酸钾在二氧化锰的催化作用和加热的条件下,受热分解能生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;氯酸钾制取氧气的反应物是固体,反应条件是加热,所以组装制取装置时,需选择如图中的ABCE;因为硫燃烧的产物二氧化硫是有毒的气体,会污染空气,因此采用排水法收集的氧气可以再集气瓶的底部留有少量的水来吸收二氧化硫;
故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;ABCE;集气瓶底部可留少量水,用于吸收硫燃烧生成的二氧化硫,防止其污染空气;
(2)根据稀释前后溶质的质量不变.
设需用20%的双氧水溶液质量为X,
20%×X=100g×6%
解之得:X=30g
所以需加水的质量为100g-30g=70g
水的体积为:70g÷1g/ml=70ml;
故答案为:70;
(3)在量取水的操作中,当水面接近所需刻度时,滴加少量的液体用胶头滴管;将配制好的溶液装入试剂瓶中,标签中的内容为溶液的名称及其质量分数;故标签中的内容应为:双氧水 6%;
故答案为:H; .
.
点评 本题综合考查了学生的基本实验能力,化学方程式的书写、装置选择、实验基本操作等知识,只有综合理解化学知识才能够正确的解答.

练习册系列答案
相关题目
1.下列实验方案能达到实验目的是( )
| A | B | C | D | |
| 方案 | 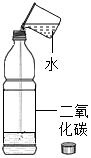 | 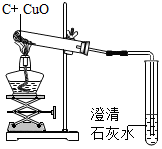 | 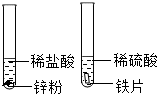 | 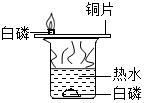 |
| 目的 | 证明二氧化碳溶于水且能和水反应 | 证明碳与氧化铜能发生反应 | 证明金属锌的活动性比铁的活动性强 | 证明燃烧的条件是温度需达到可燃物的着火点 |
| A. | A | B. | B | C. | C | D. | D |
2.在家里清洗带油污的餐具,下列哪种方法清洗最干净( )
| A. | 只用冷水 | B. | 在冷水中加几滴洗涤剂 | ||
| C. | 只用热水 | D. | 在热水中加几滴洗涤剂 |
6.从溶液的组成和性质来分析,下列物质不算作溶液的是( )
| A. | 碘酒 | B. | 酸奶 | C. | 乙醇汽油 | D. | 液态空气 |
16.“农村淘宝”里有下列多种化肥出售,其中属于复合肥料的是( )
| A. | KCl | B. | CO(NH2)2 | C. | KNO3 | D. | Ca(H2PO4)2 |
20.物质性质决定用途.下列说法正确的是( )
| A. | 可以用灼烧方法,区分棉线与蚕丝 | |
| B. | O2能支持燃烧,可作燃料 | |
| C. | 碱石灰有吸水性,可用于干燥二氧化碳 | |
| D. | 活性炭具有吸附性,可用于自来水的去色素、杀菌消毒,使自来水变成纯净物 |
1.下列化学方程式符合题意、书写及反应类型均正确的是( )
| A. | 用小苏打治疗胃酸过多:NaHCO3+HCl═NaCl+H2O+CO2↑ 中和反应 | |
| B. | 除去CO2中混有的CO,通入氧气,点燃:CO+O2$\frac{\underline{\;点燃\;}}{\;}$CO2化合反应 | |
| C. | 工业用磁铁矿炼铁:Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 置换反应 | |
| D. | 用稀硫酸除铁锈:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O 复分解反应 |