题目内容
5.称取铜、锌混合物粉末20.0g置于烧杯中,慢慢加入稀H2SO4使其充分反应,直至固体质量不再减少为止,此时用取98.0g稀H2SO4,剩余固体7.0g.(1)该混合物粉末中铜的质量是7.0g.
(2)所用稀H2SO4溶质的质量分数是多少?
分析 铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气,剩余固体的质量即为铜的质量,根据铜的质量可以计算锌的质量,根据锌的质量可以计算硫酸质量,进一步可以计算所用稀H2SO4溶质的质量分数.
解答 解:(1)该混合物粉末中铜的质量是7.0g.
故填:7.0g.
(2)设硫酸质量为x,
锌的质量为:20.0g-7.0g=13g,
Zn+H2SO4═ZnSO4+H2↑,
65 98
13g x
$\frac{65}{13g}$=$\frac{98}{x}$,
x=19.6g,
所用稀H2SO4溶质的质量分数是:$\frac{19.6g}{98.0g}$×100%=20%,
答:所用稀H2SO4溶质的质量分数是20%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
20.下列实验现象和结论都正确的是( )
| 实验操作 | 实验现象 | 实验结论 | |
| A | 将一根未打磨的铝条放入 CuSO4溶液中 | 无紫红色固体析出 | 铝不如铜活泼 |
| B | 将带火星的木条伸入O2中 | 木条复燃 | O2具有可燃性 |
| C | 将CO通过灼热的CuO | 黑色固体变成红色 | CO具有还原性 |
| D | 将CO2通入紫色石蕊试液中 | 紫色石蕊试液变成红色 | CO2具有酸性 |
| A. | A | B. | B | C. | C | D. | D |
10.下列实验操作中错误的是( )
| A. | 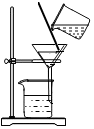 过滤溶液 | B. |  量筒的读数 | C. |  装置气密性检查 | D. |  氧气的验满 |
14.下列说法符合事实的是( )
| A. | 铁丝伸入盛有氧气的集气瓶中会剧烈燃烧 | |
| B. | 木炭粉与黑色的氧化铜粉末混合后可看到红色粉末 | |
| C. | 氢氧化钠固体放置在空气中不会变质,无需密封保存 | |
| D. | 硫燃烧后生成有刺激性气味的气体 |
 阅读材料,回答问题:
阅读材料,回答问题: