题目内容
14.向硫酸亚铁、硫酸铜的混合溶液中加入一些锌,充分反应后过滤,得固体不溶物A和滤液,将A放入少量稀硫酸中,有气体产生.则A中一定含有Cu、Fe.滤液中一定含有的溶质是ZnSO4.分析 根据金属活动性由强到弱的顺序:锌>铁>H>铜,向硫酸亚铁、硫酸铜的混合溶液中加入一些锌粉,铜首先被置换出来,待铜被完全置换后,铁开始被置换;
将过滤得到固体不溶物A放入少量的稀硫酸中,有气体产生,说明固体中有活动性较强的铁或锌,若锌过量,固体A中含有锌;若锌量不足或恰好完全反应,则固体A中不含锌;
滤液是锌与混合溶液反应后所得的溶液,且固体A中含有活动性较强的铁或锌,说明硫酸铜已完全反应,因此滤液中不含硫酸铜.
解答 解:向硫酸亚铁、硫酸铜的混合溶液中加入一些锌粉,充分反应,则所得固体A中一定含有被置换出来的铜;又固体A能与稀硫酸反应放出氢气,则固体A中一定含有铁;如果锌过量则固体A中含有锌;由于锌是否过量不能确定,所以滤液中是否还含硫酸亚铁不能确定,但可以确定的是滤液中一定不含硫酸铜,而锌与硫酸铜反应生成硫酸锌,所以滤液中一定含有硫酸锌.
故答案为:Cu、Fe;ZnSO4.
点评 金属与盐的混合溶液进行反应时,金属活动性最弱的金属首先被置换出来,然后依次按由弱到强的顺序进行置换.

练习册系列答案
相关题目
5.下列微粒符号中,对“2”含义的理解正确的是( )
| A. | 2Cu中的“2”表示2个铜元素 | |
| B. | Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷 | |
| C. | Al2(S$\stackrel{-2}{O}$4)3 中化学式上方的“2”表示硫元素为-2价 | |
| D. | H2S中的“2”表示一个硫化氢分子中含有两个硫原子 |
9.对下列现象的解释或者结论错误的是( )
| A. | “花香四溢”--分子在不断运动 | |
| B. | 在钢铁制品表面涂油漆--可防止钢铁锈蚀 | |
| C. | 向某固体中滴加稀盐酸,产生大量气泡--固体物质可能是活泼金属 | |
| D. | 把燃着的木条伸入集气瓶中,火焰熄灭--瓶中气体一定是CO2 |
19.下列水的净化方法得到的水中,纯度最高的是( )
| A. | 活性炭吸附 | B. | 过滤 | C. | 沉降 | D. | 蒸馏 |
6.根据如图,对有关物质酸碱性的比较和判断不正确的是( )


| A. | 醋的酸性最强 | B. | 西瓜汁显中性 | ||
| C. | 肥皂水的碱性最强 | D. | 苹果汁的酸性比酱油强 |
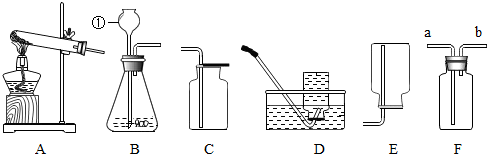
4.在日常生活中,燃烧现象屡见不鲜.你想过没有:发生燃烧的条件是什么?下面请你根据提供的物质设计实验来探究这一问题并完成下表.
实验用品:酒精灯、蜡烛、玻璃杯、镊子、水、酒精、小木条、煤块、棉花球等
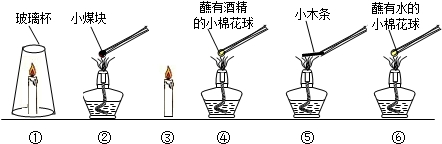
实验用品:酒精灯、蜡烛、玻璃杯、镊子、水、酒精、小木条、煤块、棉花球等

| 实验假设 | 实验内容 | 实验现象 | 实验结论 |
| 可能与物质有关 | [实验1]:(实验装置应选择④⑥) | 燃烧; 没有燃烧 | 物质燃烧必须满足的条件:物质具有可燃性 |
| 可能与 是否有氧气 有关 | [实验2]:(实验装置应选择③①)(填序号,下同) | 很快熄灭; 持续燃烧 | 要与氧气接触 |
| 可能与 着火点有关 | [实验3]:(实验装置应选择⑤②) | 点燃时间短; 点燃时间长 | 着火点低先燃烧 |
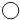 ”和“
”和“ ”分别表示两种原子,则下列各图示表示化合物的是( )
”分别表示两种原子,则下列各图示表示化合物的是( )






