题目内容
2008年北京奥运圣火在珠穆朗玛峰成功传递,假如每名运动员冲顶时消耗自带的液氧4.8 kg。求:
(1)这些氧气在标准状况下的体积是多少升?(标准状况下氧气密度为1.43 g/L)
(2)若在实验室用高锰酸钾为原料制取相同质量的氧气,需要多少千克高锰酸钾?
(3)用这种方法给登山队员供氧,是否可行?简述理由。
(1)这些氧气在标准状况下的体积是多少升?(标准状况下氧气密度为1.43 g/L)
(2)若在实验室用高锰酸钾为原料制取相同质量的氧气,需要多少千克高锰酸钾?
(3)用这种方法给登山队员供氧,是否可行?简述理由。
(1)4.8 kg氧气在标准状况下的体积为 =3 356.61。
=3 356.61。
(2)解:设需要高锰酸钾的质量为x,则有
2KMnO4=K2MnO4+MnO2+O2↑
316 32
x 4.8 kg
 ,解得x=47.4 kg
,解得x=47.4 kg
答:需要高锰酸钾的质量为47.4 kg,
(3)不行。此法成本太高,经济上不合算(或在实验室制如此多氧气,耗时太长)。
 =3 356.61。
=3 356.61。 (2)解:设需要高锰酸钾的质量为x,则有
2KMnO4=K2MnO4+MnO2+O2↑
316 32
x 4.8 kg
 ,解得x=47.4 kg
,解得x=47.4 kg 答:需要高锰酸钾的质量为47.4 kg,
(3)不行。此法成本太高,经济上不合算(或在实验室制如此多氧气,耗时太长)。

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
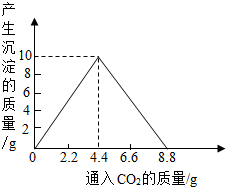 2008年5月26日上午,北京奥运圣火在我市传递.奥运祥云火炬在工艺上采用了高品质的铝合金外壳和中空塑件设计.请根据下列材料,回答有关问题:
2008年5月26日上午,北京奥运圣火在我市传递.奥运祥云火炬在工艺上采用了高品质的铝合金外壳和中空塑件设计.请根据下列材料,回答有关问题:
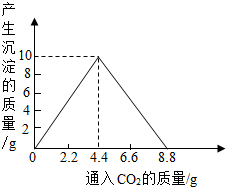 2008年5月26日上午,北京奥运圣火在我市传递.奥运祥云火炬在工艺上采用了高品质的铝合金外壳和中空塑件设计.请根据下列材料,回答有关问题:
2008年5月26日上午,北京奥运圣火在我市传递.奥运祥云火炬在工艺上采用了高品质的铝合金外壳和中空塑件设计.请根据下列材料,回答有关问题: 4Al+3O2↑.其中,冰晶石作熔剂,可使Al2O3更易离解成自由离子.冰晶石的化学式为Na3AlF6,则其中氟元素的化合价为________.
4Al+3O2↑.其中,冰晶石作熔剂,可使Al2O3更易离解成自由离子.冰晶石的化学式为Na3AlF6,则其中氟元素的化合价为________.