题目内容
14. 完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.【研究方案】先称取一定质量的氯酸钾和二氧化锰混合物、放入大试管中加热至质量不再变化为止.根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量,从而求出氯酸钾的质量.(学习小组同学事先查阅资料获知,氯酸钾分解的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,二氧化锰的质量在反应前后不变且在水中难溶.)
【解决问题】实验测得固体混合物质量随加热时间变化的相关数据如图所示.请你完成以下两个问题:
(1)反应中产生氧气多少克?
(2)原混合物中氯酸钾的质量为多少克?
分析 (1)根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量;
(2)利用氯酸钾分解的化学方程式,计算出混合物中氯酸钾的质量.
解答 解:(1)根据质量守恒定律,O2的质量为:16.0g-11.2g=4.8g;
(2)设原混合物中氯酸钾的质量为X,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
X 4.8g
∴$\frac{245}{X}$=$\frac{96}{4.8g}$,
解之得:X=12.25g;
答:(1)反应中产生氧气的质量为4.8g;(2)原混合物中氯酸钾的质量为:12.25g.
点评 本题主要考查学生利用化学方程式和质量守恒定律进行计算的能力.根据质量守恒定律,可以求出生成气体的质量,为答题打开突破口.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列实验基本操作中,正确的是( )
| A. | 用嘴吹灭酒精灯的火焰 | |
| B. | 倾倒液体时,试剂瓶上的标签向着手心 | |
| C. | 用燃着的酒精灯的火焰点燃另一个酒精灯 | |
| D. | 将带火星的木条伸入集气瓶里,检验氧气是否收集满 |
5. 表示氧原子,用○表示氢原子,则保持水的化学性质的粒子是( )
表示氧原子,用○表示氢原子,则保持水的化学性质的粒子是( )
 表示氧原子,用○表示氢原子,则保持水的化学性质的粒子是( )
表示氧原子,用○表示氢原子,则保持水的化学性质的粒子是( )| A. | 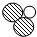 | B. | 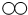 | C. | 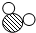 | D. |  |
2.下列选项不属于模型的是( )
| A. |  | B. |  足球烯 足球烯 | ||
| C. |  | D. | 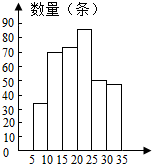 |
 水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识.请你回答:
水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识.请你回答: