题目内容
20.如表是KNO3、NaCl在不同温度下的溶解度(单位:g).| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
(2)相同温度下,若要配制KNO3和NaCl等浓度的饱和溶液,其温度范围是20℃~30℃,将50℃时等质量的KNO3和NaCl的饱和溶液分别将至20℃,析出晶体较多的是KNO3.
分析 (1)据20℃时NaCl的溶解度分析解答;50℃时,KNO3的溶解度及饱和溶液中溶质的质量分数计算式.
(2)硝酸钾和氯化钠溶解度相同的温度既是判断该段中溶解度的数值是否存在相等的可能;t2℃时,将等质量的两物质的饱和溶液分别降温至t1℃,由图可判知,析出晶体的质量KNO3>NaCl;
解答 解:(1)50℃时NaCl的溶解度是37.0g,所以向50g水中加入20gNaCl,充分溶解最多溶解18.5g,所得到溶液的质量是68.5g;溶质的质量分数是$\frac{37.0g}{100g+37.0g}$×100%=27.0%;
(2)由图可知:硝酸钾和氯化钠溶解度相同的温度既是判断该段中溶解度的数值是否存在相等的可能,经分析知在20~30℃时这两种物质存在溶解度相同的可能;将50℃时等质量的KNO3和NaCl的饱和溶液分别将至20℃,由图可判知,析出晶体的质量KNO3>NaCl;
故答案为:(1)37.0g;68.5;27.0%;(2)20℃~30℃;KNO3.
点评 本题考查了学生对溶解度、溶解度曲线及不饱和溶液和饱和溶液的相互转化等知识,掌握相关知识才能正确分析和解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.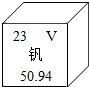 2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13),钒元素的相关信息如图.下列有关钒的说法错误的是( )
2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13),钒元素的相关信息如图.下列有关钒的说法错误的是( )
 2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13),钒元素的相关信息如图.下列有关钒的说法错误的是( )
2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13),钒元素的相关信息如图.下列有关钒的说法错误的是( )| A. | 原子的核外电子数是23 | B. | 原子核内的中子数是28 | ||
| C. | 相对原子质量为50.94 | D. | 属于稀有气体元素 |
11.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是
[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)漂白粉是一种混合物(填“纯净物”或“混合物”).
(2)HClO在常温下分解,反应为2HClO═2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小(填“增大”或“减小”或“不变”).
(3)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2 +2HCl=2HClO+CaCl2.
(4)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器:盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)漂白粉是一种混合物(填“纯净物”或“混合物”).
(2)HClO在常温下分解,反应为2HClO═2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小(填“增大”或“减小”或“不变”).
(3)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2 +2HCl=2HClO+CaCl2.
(4)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器:盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入适量盐酸,塞上带导管的单孔塞 把导管插入另一试管里的石灰水中. | 有气体产生,气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后的试管中加少量品红溶液. | 品红溶液褪色. |
15.下列生活中的说法不正确的是( )
| A. | 棉花属于有机合成材料 | |
| B. | 用灼烧法可以鉴别羊毛和晴纶 | |
| C. | 用环保布袋代替塑料袋可以减少“白色污染” | |
| D. | 石油是由多种有机物组成的复杂混合物 |
5.黄金作为一种国际流通货币,受到很多人的收藏.根据金元素在元素周期表的信息可知( )


| A. | 金是一种非金属元素 | B. | 金原子的核外电子数为79 | ||
| C. | 金原子的相对原子质量为197.0克 | D. | 金元素的符号Ag |
12.《科学》课本上是用图甲的装置来测定空气中氧气的体积分数.而小明通过查询资料对该实验进行改进,利用四硫化钠
(Na2S4)固体替代红磷进行实验,其反应原理为:
2Na2S4+O2+2H2O═8S↓+4NaOH.
实验步骤:
①将足量的四硫化钠(Na2S4)固体置于试管中,再加入适量的水并迅速塞紧橡胶塞,再充分振荡.
②测量液面至橡胶塞下沿的距离,记录数据h1(如图乙所示).
③将该试管插入水中(如图丙所示),取下橡胶塞,观察到试管内液面上升.
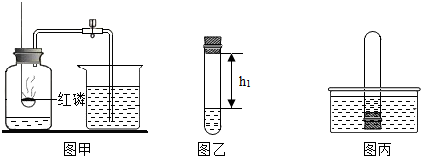
④当管内液面稳定时塞紧橡胶塞.将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2.
⑤按照①~③再重复实验2次,3次实验数据如表所示.
(1)步骤①中进行充分振荡的目的是使反应物充分反应.
(2)根据3次实验数据,请你计算空气中氧气的体积分数为20.9%(结果精确到0.1%);
(3)小明设计的实验与课本上的实验相比,其优点是节能、装置简单、气密性好等.(写出2点)
(Na2S4)固体替代红磷进行实验,其反应原理为:
2Na2S4+O2+2H2O═8S↓+4NaOH.
实验步骤:
①将足量的四硫化钠(Na2S4)固体置于试管中,再加入适量的水并迅速塞紧橡胶塞,再充分振荡.
②测量液面至橡胶塞下沿的距离,记录数据h1(如图乙所示).
③将该试管插入水中(如图丙所示),取下橡胶塞,观察到试管内液面上升.

④当管内液面稳定时塞紧橡胶塞.将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2.
⑤按照①~③再重复实验2次,3次实验数据如表所示.
| 第1次 | 第2次 | 第3次 | |
| h1/厘米 | 11.0 | 11.4 | 11.6 |
| h2/厘米 | 8.7 | 9.1 | 9.2 |
(2)根据3次实验数据,请你计算空气中氧气的体积分数为20.9%(结果精确到0.1%);
(3)小明设计的实验与课本上的实验相比,其优点是节能、装置简单、气密性好等.(写出2点)
10.除去下列物质或溶液中少量杂质(括号内为杂质)的方法,合理可行的是( )
| 选项 | 物质 | 操作方法 |
| A | 氧化钙(碳酸钙) | 加水、过滤 |
| B | 氯化亚铁(氯化铜) | 加足量铁粉、过滤 |
| C | 硫酸(盐酸) | 加入适量硝酸银溶液、过滤 |
| D | 二氧化碳(氧气) | 用带火星的木条点燃气体 |
| A. | A | B. | B | C. | C | D. | D |