题目内容
19.M2SO4•xH2O是一种中药,具有通便、清火消肿的功效,其中M是一种金属元素,x是数字,M2SO4•xH2O的相对分子质量为322.现将16.1gM2SO4•xH2O加热至完全失去结晶水,变为M2SO4粉末,质量减少9g.[提示:CuSO4•5H2O的相对分子质量计算式为:64+32+16×4+5×(1×2+16)=250]
试回答下列问题:
(1)M是Na(填元素符号);
(2)x为10;
(3)M2SO4中硫、氧两种元素的质量比为1:2.
分析 根据M2SO4•xH2O受热分解为M2SO4和H2O,以及质量的变化情况结合化学方程式进行计算;
根据化合物中元素质量比的计算方法来分析.
解答 解:由题干信息可知:
M2SO4•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$M2SO4+xH2O
322 18x
16.1g 9g
$\frac{322}{18x}=\frac{16.1g}{9g}$
x=10
设元素M的相对原子质量为m,因为M2SO4•xH2O的相对分子质量为322,所以2m+32+16×4+10×(1×2+16)=322
m=23
则M元素是钠元素.
Na2SO4中硫、氧两种元素的质量比为:32:(16×4)=1:2.
故答案为:(1)Na;(2)10;(3)1:2.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
7.下列有关物质燃烧现象的描述,不正确的是( )
| A. | 磷在空气中燃烧产生大量白烟 | |
| B. | 镁条在空气中燃烧发出耀眼的白光 | |
| C. | 氢气在空气中燃烧发出淡蓝色火焰 | |
| D. | 铁丝在氧气中燃烧火星四射,生成黑色的四氧化三铁 |
14.如图是元素X的原子结构示意图.下列说法正确的是( )
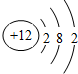

| A. | 该原子在化学变化中易得电子 | B. | X属于非金属元素 | ||
| C. | X与Cl形成的化合物为XCl2 | D. | 该原子最外电子层达到了稳定结构 |
11.在一个密闭容器中由X、Y、Z、Q四种物质,一定条件下充分反应,测量反应前后各物质的质量如下表所示,下列推理正确的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 8 | 10 | 1 | 21 |
| 反应后质量/g | 0 | 21 | 未测 | 9 |
| A. | 反应后反应物质Z的质量为9g | |
| B. | 反应后物质Y和Q发生改变的质量之比为1:1 | |
| C. | 反应中生成的Y的质量为21g | |
| D. | 若Q为氧气,则该反应为氧化反应 |
8.在一只透明的玻璃杯里装入半杯水,向其中加入一块冰糖,盖上盖子,立即在液面处画上记号,过一段时间,观察到冰糖消失、液面下降.这一实验说明( )
| A. | 糖溶于水是化学变化 | B. | 分子在不停地运动 | ||
| C. | 分子间有间隔 | D. | 分子会破裂成原子 |
9.下列关于水的叙述中,描述的是水的化学性质的是( )
| A. | 降温到0℃,水结成冰 | B. | 加热到100℃,水变成水蒸气 | ||
| C. | 给水通电,会生成氢气和氧气 | D. | 水蒸气遇冷,凝结成水 |
