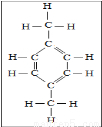
题目内容
(17分)为粗略测定空气中SO2的含量,某学习小组设计了如下图所示的实验装置进行实验。
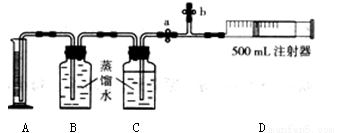
【资料】
①室温下,碘的溶解度为0.029g。
②我国空气质量标准中SO2浓度限值(mg/m3)如下表。
一级标准 | 二级标准 | 三级标准 |
1≤0.15 | ≤0.50 | 0 ≤0.70 |
③SO2+I2+2H2O===H2SO4+2HI。
④SO2可以使酸性KMnO4溶液褪色。
【实验步骤】
①检查气密性;②向C装置中加入1.0 mL溶质质量分数为1.27×10“g/mL的碘水(ρ≈1.0g/mL),滴入2~3滴淀粉溶液;③打开弹簧夹____(填“a”或“b”),关闭另一个弹簧夹,抽拉注射器吸取500 mL空气,再开、闭相应弹簧夹,缓缓推气体进入C装置,重复上述操作多次。当C中溶液颜色____时,停止推动注射器的活塞;④实验数据处理。
请回答下列问题。
(1)完善步骤③的内容:_____________;____________;
(2)检查装置气密性的操作是____,若____,说明装置的气密性良好;
(3)实验时,C装置中原有蒸馏水对实验有无影响?____(填“有影响”或“无影响”);在下列因素中,会使测定结果偏低的是____。
A.推动注射器活塞速率太快
B.长期放置的碘水溶质质量分数低于1.27×10-6g/mL
C.抽取空气时,未抽满500 mL
(4)以下试剂可以代替C装置中碘的淀粉溶液的是____。
A.NaOH溶液 B.酸性KMnO4溶液 C.蒸馏水 D.酚酞试液
(5)工业上吸收SO2常用足量氨水(用NH3·H2O表示),生成一种相对分子质量为116的盐,反应的化学方程式为______________;还可用石灰乳[Ca(OH)2悬浊液]吸收SO2获得副产品石膏,请补充完整该反应方程式:2SO2+O2+2Ca(OH)2+2H2O===2________。
(6)该小组在同一地点进行了3次实验,推动活塞次数记录如下表(每次抽气为500 mL)。进行3次实验的目的是____;综合3次实验数据分析:该测定地点的空气质量属于____级标准(写出计算过程)。
实验序号 | 1 | 2 | 3 |
推动次数 | 19 | 20 | 21 |
(1)b 由蓝色变成无色(或褪色)
(2)关闭弹簧夹b,打开弹簧夹a,将注射器活塞从右向左推A中得到水的体积等于注射器活塞推动的体积(或轻推注射器,C中有气泡,且B中导管内形成稳定液柱。其他合理答案也可,体积相等)
(3)无影响 AC (4)B
(5)SO2+2NH3·H2O===(NH4)2SO3+H2O CaSO4·2H2O
(6)取平均值,使测定结果更准确 一
【解析】
试题分析:(1)打开弹簧夹b关闭另一个弹簧夹,抽拉注射器吸取500 mL空气, 当C中溶液颜色由蓝色变成无色(或褪色)时,停止推动注射器的活塞
(2)检查装置气密性的操作是:关闭弹簧夹b,打开弹簧夹a,将注射器活塞从右向左推A中得到水的体积等于注射器活塞推动的体积,说明装置的气密性良好(或轻推注射器,C中有气泡,且B中导管内形成稳定液柱。其他合理答案也可,体积相等)
(3)实验时,C装置中原有蒸馏水对实验无影响;A、推动注射器活塞速率太快,这样空气中SO2的来不及反应就直接排出,使得测定结果偏低,正确,B、长期放置的碘水溶质质量分数低于1.27×10-6g/mL,这样使得消耗的空气体积偏小,使测定结果偏高,C、抽取空气时,未抽满500 mL,这样就等于减少了二氧化硫的量,这样使得测定结果偏低,正确,故选AC
(4)根据信息,二氧化硫还能使高锰酸钾溶液褪色,故选B
(5)工业上吸收SO2常用足量氨水(用NH3·H2O表示),生成一种相对分子质量为116的盐,结合质量守恒定律,可以推出为:(NH4)2SO3,故反应的化学方程式为:SO2+2NH3·H2O===(NH4)2SO3+H2O; 根据反应方程式:2SO2+O2+2Ca(OH)2+2H2O===2CaSO4·2H2O
(6)进行3次实验的目的是取平均值,使测定结果更准确
解:3次实验活塞平均推动次数(19+20+21)次/3=20次
注射器每次抽气体积为20次×500 mL/次=10000 mL
SO2 ~ I2
64 254
x l.27×10-6g/mL×l.0 mL
64:254= x:l.27×10-6g/mL×l.0 mL
解得x=0.32×10-6g
该测定地点空气中SO2浓度为=0.32×10-6g /10000 mL =0.032 mg/m3
结论:该测定地点的空气质量为一级标准
考点:装置气密性的检查,质量守恒定律的应用,化学方程式的书写,根据化学方程式极性的计算

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案(10分)通过实验对草酸(相对分子质量是90)进行如下研究。
【查阅资料】①浓硫酸常作干燥剂 ②浓NaOH溶液常用于吸收CO2气体
③无水硫酸铜吸水后由白色变为蓝色 ④氯化钯(PdCl2)溶液遇CO产生黑色沉淀
【实验准备】选用下列实验装置(气密性良好,部分固定装置已略去):
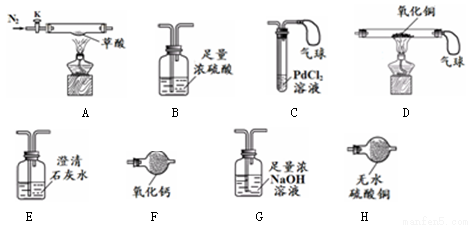
【实验I】检验草酸分解的产物。
实验步骤 | 实验现象 | 实验结论及分析 |
(1)按A→H→E→C 连接仪器 (2)关闭K,点燃A处酒精灯 | H中 E中澄清石灰水变浑浊 C中产生黑色沉淀,气球鼓起 | 草酸分解生成了CO2、CO和H2O ①E中反应的化学方程式是 ②C中气球的作用是 |
【实验II】取9 g草酸进行实验,测定生成物的质量并确定草酸的组成。
实验步骤 | 实验数据 | 实验结论及分析 |
(1)选择A、B、D、G装置组合进行实验 (2)鼓入过量的N2后,分别称量B、D、G的质量 (3)关闭K,点燃A、D处的酒精灯,至草酸完全分解 (4)熄灭A处酒精灯,通入过量的N2,熄灭D处酒精灯,再次分别称量B、D、G的质量 | B装置增重1.8 g D装置中固体 质量减少0.8 g G装置增重4.4 g | ①A、B、D、G装置的正确连接顺序是A→ → →D ②向A中两次通入N2,其中 第二次的目的是 ③草酸的化学式是 ④反思:若用F代替B,则不能测定草酸的组成,其原因是 |