题目内容
炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见图:
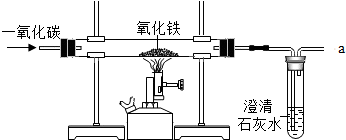
对实验进行分析并回答:
(1)实验中玻璃管里氧化铁粉末的颜色变化是 .观察到澄清石灰水的现象是 ,反应的化学方程式为 .
(2)实验前“通入CO”与“开始加热”的顺序是 .
(3)从环保角度分析,该流程设计中的一处明显不足是 .

对实验进行分析并回答:
(1)实验中玻璃管里氧化铁粉末的颜色变化是
(2)实验前“通入CO”与“开始加热”的顺序是
(3)从环保角度分析,该流程设计中的一处明显不足是
考点:一氧化碳还原氧化铁,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据反应物和生成物,分析实验中玻璃管里氧化铁粉末的颜色变化.根据二氧化碳能与氢氧化钙反应分析澄清石灰水的现象,书写化学方程式;
(2)根据玻璃管内有空气,通入一氧化碳易发生爆炸分析;
(3)根据一氧化碳是对大气有污染的气体分析.
(2)根据玻璃管内有空气,通入一氧化碳易发生爆炸分析;
(3)根据一氧化碳是对大气有污染的气体分析.
解答:解:
(1)由于在高温下,一氧化碳将氧化铁还原为铁,同时生成了二氧化碳.所以,实验中玻璃管里氧化铁粉末的颜色变化是红色粉末变黑色;二氧化碳能与氢氧化钙反应生成了碳酸钙沉淀和水.所以,观察到澄清石灰水的现象是:石灰水变浑浊;而反应的化学方程式为 CO2+Ca(OH)2═CaCO3↓+H2O.
(2)由于玻璃管内有空气,通入一氧化碳高温时易发生爆炸.所以实验前先通入CO,排净玻璃管中的空气再开始加热.
(3)为了防止一氧化碳对大气的污染,所以实验时要在装置末端a处燃着一盏酒精灯除去反应剩余的CO.
故答案为:(1)红色粉末变黑色; 石灰水变浑浊; CO2+Ca(OH)2═CaCO3↓+H2O
(2)先通入CO再开始加热;
(3)没有尾气处理(吸收)装置;
(1)由于在高温下,一氧化碳将氧化铁还原为铁,同时生成了二氧化碳.所以,实验中玻璃管里氧化铁粉末的颜色变化是红色粉末变黑色;二氧化碳能与氢氧化钙反应生成了碳酸钙沉淀和水.所以,观察到澄清石灰水的现象是:石灰水变浑浊;而反应的化学方程式为 CO2+Ca(OH)2═CaCO3↓+H2O.
(2)由于玻璃管内有空气,通入一氧化碳高温时易发生爆炸.所以实验前先通入CO,排净玻璃管中的空气再开始加热.
(3)为了防止一氧化碳对大气的污染,所以实验时要在装置末端a处燃着一盏酒精灯除去反应剩余的CO.
故答案为:(1)红色粉末变黑色; 石灰水变浑浊; CO2+Ca(OH)2═CaCO3↓+H2O
(2)先通入CO再开始加热;
(3)没有尾气处理(吸收)装置;
点评:本题主要考查一氧化碳与氧化铁反应实验装置、实验现象、一氧化碳的化学性质和污染,属基础性知识考查题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关于水的认识正确的是( )
| A、电解水可以得到氧气,是因为水中溶有氧气 |
| B、氧气和氢气反应生成水,说明水是由氢气和氧气组成的 |
| C、经过沉淀、过滤后得到的矿泉水是纯净物 |
| D、自来水的净化通常要经过沉淀、过滤、杀菌消毒等过程 |
下列叙述正确的是( )
| A、服用氢氧化钠可治疗胃酸过多 |
| B、酸雨就是指呈酸性的雨水,所以正常雨水为酸雨 |
| C、稀盐酸可以除去水壶中的水垢 |
| D、pH=0的溶液是中性溶液 |
用托盘天平称量固体药品时,将药品和砝码位置放置颠倒了,天平平衡后,砝码为5g,游码为0.5g,药品的质量是( )
| A、5.5g | B、5g |
| C、4.5g | D、0.5g |
 用如图的装置探究二氧化碳的制取和性质.下列关于该探究实验的叙述正确的是( )
用如图的装置探究二氧化碳的制取和性质.下列关于该探究实验的叙述正确的是( )| A、粗铜丝能控制反应的发生和停止 |
| B、浸有紫色石蕊试液的棉花会变蓝 |
| C、可以将粗铜丝换成铁丝 |
| D、能验证二氧化碳的密度比空气大 |