题目内容
6.某实验小组的同学用稀硫酸、铁丝、铜丝三种试剂来测定铁、铜金属活动性.在做实验时,他们发现了一个有趣的现象.如图所示,甲图中看到在铜片的表面有气泡产生,而乙图中看到在铁片的表面有气泡产生.同学们产生了很大的疑问,这是怎么回事呢?带着疑问,同学们查阅了大量的资料,并请教了老师.
[查阅资料]甲图中反应的化学方程式为:Fe+H2SO4═H2+FeSO4.出现氢气在铜片放出的原因是由于铁和铜连接在一起,形成了原电池,原电池是一种把化学能转化为电能的装置,在甲图中铁失去电子变成亚铁离子,它失去的电子会从铁片运动到铜片,而溶液中的氢离子只有在铜片的表面才能得到电子变成氢原子,而后再结合生成氢气分子放出.
[实验探究]学到了新知识,同学们于是决定依据该原理重新做一个实验,如图丙,他们把稀硫酸溶液换成硫酸铜溶液重新进行实验.该反应现象为铜片表面附着一层红色固体;该反应的化学方程式为Fe+CuSO4═FeSO4+Cu.从微观的角度说明其化学反应的本质为铁原子失去电子变成亚铁离子,铜离子得到电子变成铜原子.
分析 铁和稀硫酸反应生成硫酸亚铁和氢气,和硫酸铜反应生成硫酸亚铁和铜;
铁和硫酸铜反应的微观实质是:铁原子失去电子变成亚铁离子,铜离子得到电子变成铜原子.
解答 解:把稀硫酸溶液换成硫酸铜溶液重新进行实验时,该反应现象为铜片表面附着一层红色固体;
该反应中,铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;
从微观的角度说明其化学反应的本质为是:铁原子失去电子变成亚铁离子,铜离子得到电子变成铜原子.
故填:铜片表面附着一层红色固体;Fe+CuSO4═FeSO4+Cu;铁原子失去电子变成亚铁离子,铜离子得到电子变成铜原子.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
14.我国有许多盐碱湖,湖水中溶有大量的氯化钠和纯碱,那里的农民冬天捞碱、夏天晒盐,试用你学过的知识说明其中的道理(不同温度下相关的溶解度数据下表).
| 温度(℃) | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
| 氯化钠(克) | 35.7 | 35.8 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 温度(℃) | 0 | 10 | 20 | 30 | … | 90 | |
| 纯碱(克) | 7.1 | 12.5 | 21.5 | 38.8 | … | 43.9 | |
1.某溶液中只含有Na+、Al3+、Cl-、SO42- 四种离子,已知前三种离子的个数比为3:2:1,则溶液中Al3+和 SO42-的离子个数比为( )
| A. | 1:2 | B. | 1:4 | C. | 3:4 | D. | 3:2 |
11.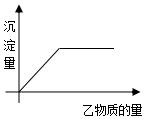 向甲物质中加入(或通入)乙物质,生成的沉淀量与所用的乙物质的量关系如图,则表中不符合条件的一组是( )
向甲物质中加入(或通入)乙物质,生成的沉淀量与所用的乙物质的量关系如图,则表中不符合条件的一组是( )
 向甲物质中加入(或通入)乙物质,生成的沉淀量与所用的乙物质的量关系如图,则表中不符合条件的一组是( )
向甲物质中加入(或通入)乙物质,生成的沉淀量与所用的乙物质的量关系如图,则表中不符合条件的一组是( )| 组别 | 甲 | 乙 |
| A | FeCl3溶液 | NaOH溶液 |
| B | NaOH溶液 | CO2气体 |
| C | CuSO4溶液 | BaCl2 |
| D | 一定量海水 | AgNO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
16.某小组以稀硫酸与氢氧化钠溶液是否能发生反应为课题进行研究.同学向烧杯中的氢氧化钠溶液加入稀硫酸,一会发现忘记滴加指示剂,因此他们停止滴加稀硫酸,并对烧杯内稀硫酸和氢氧化钠溶液是否发生反应进行探究.
(1)小组同学设计了以下实验方案:
(2)写出该反应的化学方程式:2NaOH+H2SO4═Na2SO4+2H2O
(3)同学们一致讨论认为,不用上述方法,用其他试剂也可以证明稀硫酸与氢氧化钠溶液能发生反应,于是分成甲乙两组实验.
甲组实验:探究CuSO4溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应.
操作及现象:向氢氧化钠溶液中加入足量稀硫酸时无明显现象,再滴加CuSO4溶液时没有出现沉淀.
结论:通过以上实验,你认为用CuSO4溶液可以(填可以或不可以)证明稀硫酸与氢氧化钠溶液能发生反应.
乙组实验:探究BaCl2溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应.
操作及现象:向稀硫酸中加入足量氢氧化钠溶液时无明显现象,再滴加BaCl2溶液时出现白色沉淀.
结论:通过以上实验,你认为用BaCl2溶液不可以(填可以或不可以)证明稀硫酸与氢氧化钠溶液能发生反应.理由是:稀硫酸、硫酸钠都会电离出硫酸根离子,硫酸根离子都会与钡离子生成硫酸钡沉淀.
(1)小组同学设计了以下实验方案:
| 实验步骤 | 实验现象 | 实验结论 |
| 在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量反应后的溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,读溶液的pH | pH<7 (填“>”、“=”或“<”) | 稀硫酸与氢氧化钠溶液发生了反应,且稀硫酸过量了. |
(3)同学们一致讨论认为,不用上述方法,用其他试剂也可以证明稀硫酸与氢氧化钠溶液能发生反应,于是分成甲乙两组实验.
甲组实验:探究CuSO4溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应.
操作及现象:向氢氧化钠溶液中加入足量稀硫酸时无明显现象,再滴加CuSO4溶液时没有出现沉淀.
结论:通过以上实验,你认为用CuSO4溶液可以(填可以或不可以)证明稀硫酸与氢氧化钠溶液能发生反应.
乙组实验:探究BaCl2溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应.
操作及现象:向稀硫酸中加入足量氢氧化钠溶液时无明显现象,再滴加BaCl2溶液时出现白色沉淀.
结论:通过以上实验,你认为用BaCl2溶液不可以(填可以或不可以)证明稀硫酸与氢氧化钠溶液能发生反应.理由是:稀硫酸、硫酸钠都会电离出硫酸根离子,硫酸根离子都会与钡离子生成硫酸钡沉淀.