题目内容
氧化铜和炭粉的混合物10g加热后充分反应,一段时间后冷却,称得剩余固体质量为7.8g,试求原混合物中参加反应的氧化铜是多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据碳粉和氧化铜反应生成铜和二氧化碳,所以反应前后固体减少的质量就是二氧化碳的质量,利用方程式即可求出氧化铜的质量.
解答:解:根据碳粉和氧化铜反应生成铜和二氧化碳,所以反应前后固体减少的质量就是二氧化碳的质量,二氧化碳的质量=10g-7.8g=2.2g.
设原混合物中参加反应的氧化铜的质量是x.
2CuO+C
2Cu+CO2↑
160 44
x 2.2g
=
x=8g
答:原混合物中参加反应的氧化铜的质量是8g.
设原混合物中参加反应的氧化铜的质量是x.
2CuO+C
| ||
160 44
x 2.2g
| 160 |
| x |
| 44 |
| 2.2g |
x=8g
答:原混合物中参加反应的氧化铜的质量是8g.
点评:此题是依据化学方程式计算的基础考查题,解题的关键是反应前后固体减少的质量就是二氧化碳的质量.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列哪种物质溶于水制得的冰袋可用高烧病人降温( )
| A、食盐 | B、硝酸铵 |
| C、蔗糖 | D、生石灰 |
下列物质的用途主要由物理性质决定的是( )
| A、镁粉用于制作照明弹 |
| B、石墨用作电池的电极 |
| C、氧气用于急救病人 |
| D、氮气用作粮食的保护气 |
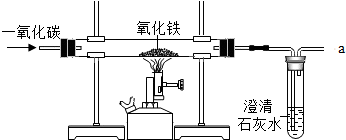
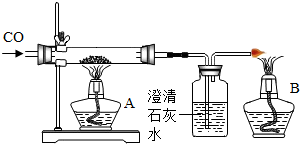
 国家环保总局已规定将各类实验室纳入环保监管范围.某中学九年级甲、乙两个班的同学分别做常见酸和碱与指示剂反应的实验,所做的实验和使用的试剂如图所示.实验后废液分别集中到各班的废液缸中,甲班废液呈红色,乙班废液呈蓝色.请你分析废液的成分:甲班废液含有
国家环保总局已规定将各类实验室纳入环保监管范围.某中学九年级甲、乙两个班的同学分别做常见酸和碱与指示剂反应的实验,所做的实验和使用的试剂如图所示.实验后废液分别集中到各班的废液缸中,甲班废液呈红色,乙班废液呈蓝色.请你分析废液的成分:甲班废液含有