��Ŀ����
18��������Na2CO3��Һ���뵽һ����CuSO4��Һ�еõ���ɫ���壮ij�о���ѧϰС�����ɫ����ijɷֽ���������̽������������и��⣺��������裺
����һ������ΪCuCO3�����ɣ�Na2CO3+CuSO4=CuCO3��+Na2SO4���û�ѧ��Ӧ����ʽ��ʾ����
�����������ΪCu��OH��2�����ɣ�Na2CO3��Һ�ʼ��ᡱ����ԣ�
������������ΪCu��OH��2��CuCO3�Ļ���
�����ϲ��ģ�
��Cu��OH��2��CuCO3����������ᾧˮ����ˮ����ͭ�ǰ�ɫ���壬��ˮ������ɫ������ͭ���壮��Cu��OH��2��CuCO3�����ֽ⣬�����ɶ�Ӧ�����������
�������ʵ�飺
�����Ļ�ȡ��
��1������Ӧ��Ĺ̡�Һ����ᆳ���ˡ�ϴ�ӡ����º�ɵ���ɫ���壮
��2���жϹ�����ϴ���ķ���������ȡ���ϴ��Һ�������μ�������ϡ���ᣬ�����ݲ�����
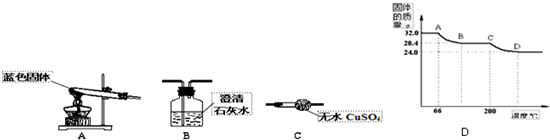
������ͼ��ʾװ�ã�����̽������ijɷ֣�
��3��С��ͬѧ��װ�ð� A��C��B���B������C����˳����Ͻ���ʵ�飬��֤������������ȷ�ģ�ʵ���У�A�е�����Ϊ��ɫ������ɺ�ɫ��C�е�����Ϊ��ɫ���������
���ۣ�����ΪCu��OH��2��CuCO3�Ļ���
�����ɷֶ����ⶨ��
��֪Cu��OH��2�ķֽ��¶�Ϊ66�桫68�棬CuCO3�ķֽ��¶�Ϊ200�桫220�森���������ΪaCu��OH��2•bCuCO3��С��ͬѧ���ȷ����ǶԹ�������ȷֽ⣬���������ݣ���ɹ��������仯��ֽ��¶ȵĹ�ϵ��ͼD�������ͼʾ�ش��������⣺
��4��д��AB��CD�η�����Ӧ�Ļ�ѧ����ʽ��
AB��Cu��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CuO+H2O��
CD��CuCO3$\frac{\underline{\;\;��\;\;}}{\;}$CuO+CO2����
��5��ͨ������ɵã�a��b=2��1������д��������̣�
���� ��һ����������裺����Na2CO3��Һ���뵽һ����CuSO4��Һ�еõ���ɫ���壬̼������ˮ��ˮ��IJ�����з�����
���������ʵ�飺
��2������̼���ƻ������ᷴӦ���ɶ�����̼���з�����
��3��������ˮ����ͭ��ˮ�������з�����
��4�����ݼ���ˮҪ���ڼ��������̼��ǰ����з�����
��5������������ͭ��̼��ͭ�ķֽ��¶Ƚ��з���������������ͭ��̼��ͭ�ֽ�Ļ�ѧ����ʽ���з�����
��� �⣺��һ����������裺̼����������ͭ��Ӧ�����������ƺ�̼��ͭ��̼��ͭΪ��ɫ���壬�ʲ���һ������ΪCuCO3�������ǣ�Na2CO3+CuSO4=CuCO3��+Na2SO4��̼������ǿ�������Σ���ˮ��ˮ�����������������ӣ���Ϊ���
�����������ʵ�飺
��2�������ϲ�����̼���ƻ������ᷴӦ���ɶ�����̼���壻�ʴ�Ϊ��ȡ���ϴ��Һ�������μ�������ϡ���ᣬ�����ݲ�����
��3������ˮҪ���ڼ��������̼��ǰ�棬����ͨ��ʯ��ˮʱЯ����ˮ������Լ���ˮ�������ţ�ʵ���У�A�е�����Ϊ����ɫ������ɺ�ɫ��C�а�ɫ�������ɫ���ʴ�Ϊ��C��B����ɫ������ɺ�ɫ����ɫ�������ɫ��
��4��AB�ε��¶ȴ���60�浫��û�г���200�棬��ͼ���п���Ҳ������100�棬�������������ķֽ��¶ȣ��ʴ�Ϊ��Cu��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CuO+H2O��
CD�ε��¶ȳ�����200�棬����̼��ͭ�ķֽ��¶ȣ��ʴ�Ϊ��CuCO3$\frac{\underline{\;\;��\;\;}}{\;}$CuO+CO2����
��5��AB����������ͭ�ڷֽ⣬������������3.6�ˣ�CD����̼��ͭ�ڷֽ⣬������������4.4�ˣ��ӷ���ʽ���Կ���һ��������ͭ�ֽ������һ��ˮ����AB�ε�������ͭ������3.6��ˮ��������0.2��ˮ��������������ͭ�ĸ���Ϊa
Cu��OH��2 $\frac{\underline{\;\;��\;\;}}{\;}$CuO+H2O
1 18
a 3.6g
a=$\frac{1��3.6}{18}$=0.2��
CD��һ��̼��ͭ�ֽ�����һ��������̼����̼��ͭ�ֽ�������4.4�˶�����̼����̼����4.4�˶�����̼��b��̼��ͭ��
CuCO3$\frac{\underline{\;\;��\;\;}}{\;}$CuO+CO2����
1 44
b 4.4
Y=$\frac{1��4.4}{44}$=0.1����a��b=0.2��0.1=2��1���ʹ�������aCu��OH��2•bCuCO3��a��b=2��1��
�ʴ�Ϊ�����������
Na2CO3+CuSO4=CuCO3��+Na2SO4���
�������ʵ��
��2��ȡ���ϴ��Һ�������μ�������ϡ���ᣬ�����ݲ���
��3��C B����1�֣� ��ɫ������ɺ�ɫ����ɫ���������
��4��Cu��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CuO+H2O�� CuCO3$\frac{\underline{\;\;��\;\;}}{\;}$CuO+CO2����
��5��2��1��
���� �ڽ������ʱ������Ҫ�����е�֪ʶ��֪��Ȼ����ѧ����֪ʶ���н�𣬴������ѶȽϴ�Ҫϸ�Ľ��з������

 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�| A�� | ��ʳ�����յ��߲ˡ��㡢���ʳƷ����ζ���أ��������ӳ�����ʱ�� | |
| B�� | ��·�ϵĻ�ѩ�������Ȼ��������� | |
| C�� | С�մ�������θ������ҩ��֮һ | |
| D�� | ��������Һ���һ���ܷ������ֽⷴӦ |
������ʵ�顿
| ʵ����� | ʵ������ | ʵ����� | |
| ��1�� | �ֱ���A��B��C��֧�Թ�ȡ������Һ��������Ȼ���ٸ�����һ������̼������Һ | A�г��ְ�ɫ���� B������������ C������������ | A�е�ԭ��Һ���Ȼ�����Һ B�е�ԭ��Һ��ϡ���� C�е�ԭ��Һ������������Һ |
| ʵ����� | ʵ������ | ʵ����� | |
| ��2�� | ȡ������Һ���Թ��У������м����������Ȼ�����Һ�����ˣ��ó�������Һ��������м�������ϡ���ᣮ | ������ɫ��������ɫ����������ʧ | ����ʵ�������֪����Һ�к���Na2CO3 ��Na2SO4����д���ʵĻ�ѧʽ�� |
| ��3�� | ȡ������Һ���Թ��У�����������̪ | ��Һ��� | ����ʵ�������֪����Һ�к����������� |
| A�� | �������е����� | B�� | ͭ�ڿ����������ܱ�� | ||
| C�� | ���ʯ��Ӳ | D�� | �ƾ��ӷ� |

 2012��3��22�ǵڶ�ʮ�조����ˮ�ա���ˮ����������������������أ�
2012��3��22�ǵڶ�ʮ�조����ˮ�ա���ˮ����������������������أ�