题目内容
14.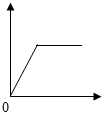 如表中的选项不符合图中所示曲线的是( )
如表中的选项不符合图中所示曲线的是( )| 选项 | 横坐标 | 纵坐标 |
| A | 向一定量稀硫酸中加入锌粉的质量 | 产生氢气的体积 |
| B | 向一定量的氢氧化钠和碳酸钠混合溶液中加入稀盐酸的质量 | 产生气体的质量 |
| C | 向一定量的澄清石灰水中加入碳酸钠溶液的质量 | 生成沉淀的质量 |
| D | 在一定温度下,向一定量的水中加入食盐晶体的质量 | 溶液中溶质的质量分数 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据锌和硫酸在常温下的反应分析.
B、在碱存在的环境下,加入酸后酸首先要与碱反应而后再和盐发生反应,据此分析即可.
C、氢氧化钙能与碳酸钠反应生成碳酸钙的沉淀,据此分析即可;
D、在一定温度下,向水中加入食盐晶体,食盐会溶解,但是当达到饱和时就不在溶解了;
解答 解:A、锌和硫酸在常温下就可反应,并且是只要接触就会反应,氢气质量上升直至反应结束,所以曲线的起点应该在原点,最终形成一条水平线,氢气量不再增加,故符合.
B、向一定量的氢氧化钠和碳酸钠混合溶液中加入稀盐酸时,稀盐酸先要与氢氧化钠反应而后再与碳酸钠反应,故产生气体的曲线的起始点不在原点,故不符合.
C、向一定量的澄清石灰水中加入碳酸钠溶液的质量时,由于氢氧化钙能与碳酸钠反应生成碳酸钙的沉淀,所以沉淀量从起点不断增加,直至反应结束,故符合.
D、在一定温度下,向水中加入食盐晶体,食盐会溶解,但是当达到饱和时就不在溶解了,那么溶液的质量也不再增加了,此时溶质的质量分数也不再改变,由于是向水中加入的食盐,所以曲线的起点应该是原点,故符合.
故选B.
点评 本题考查的是物质的化学反应与函数图象相结合的知识,在完成这类题目时,要注意分析化学反应发生的情况,然后看能否与函数图象相符合.

练习册系列答案
相关题目
4.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | HCl(CO2) | 适量NaOH溶液 | 洗气 |
| B | NaCl(NaOH) | 过量稀盐酸 | 蒸发结晶 |
| C | CO2(CO) | 足量O2 | 点燃 |
| D | 稀盐酸(稀硫酸) | 适量锌粒 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
5.配制5%的氯化钠溶液,用量筒量取水时,仰视刻度,则所得溶液的质量分数为( )
| A. | 等于5% | B. | 大于5% | C. | 小于5% | D. | 无法判断 |
2.下列生活中的各物质属于纯净物的是( )
| A. | 蒸馏水 | B. | 自来水 | C. | 碳酸饮料 | D. | 糖水 |
9.如图为某反应的微观示意图,不同的球代表不同元素的原子,下列说法中错误的是( )
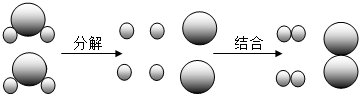

| A. | 该反应的反应物属于氧化物 | B. | 该反应类型为分解反应 | ||
| C. | 该反应可以用于实验室制取氧气 | D. | 该反应发生的条件是通电 |
19.下列各组含氮元素的物质中,氮元素化合价相同的一组是( )
| A. | N2 HNO3 | B. | NO2 Na2NO2 | C. | Na2NO2 N2O5 | D. | N2O5 Ca(NO3)2 |
6.下列除去杂质的方法错误的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | MnO2(KCl) | 加水溶解、过滤、洗涤、干燥 |
| B | CaO(CaCO3) | 高温煅烧至固体质量不再改变 |
| C | N2(O2) | 通过灼热的足量的铜网 |
| D | CO2(CO) | 通入氧气,点燃 |
| A. | A | B. | B | C. | C | D. | D |
3.推理是化学学习中常用的思维方法,下列推理中正确的是( )
| A. | 碱溶液能跟某些非金属氧化物反应,所以碱溶液能吸收CO气体 | |
| B. | 置换反应生成单质和化合物,但是有单质和化合物生成的反应不一定是置换反应 | |
| C. | 溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 | |
| D. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 |
4. 美国两位科学家通过对碘元素的研究,揭示了“细胞如何感知周围环境”之谜,从而获得诺贝尔化学奖,下列有关说法错误的是( )
美国两位科学家通过对碘元素的研究,揭示了“细胞如何感知周围环境”之谜,从而获得诺贝尔化学奖,下列有关说法错误的是( )
 美国两位科学家通过对碘元素的研究,揭示了“细胞如何感知周围环境”之谜,从而获得诺贝尔化学奖,下列有关说法错误的是( )
美国两位科学家通过对碘元素的研究,揭示了“细胞如何感知周围环境”之谜,从而获得诺贝尔化学奖,下列有关说法错误的是( )| A. | 碘的核电荷数是53 | |
| B. | 碘元素位于元素周期表中第五周期 | |
| C. | 碘元素与氯元素具有相似的化学性质 | |
| D. | 碘原子的中子数约为127 |