题目内容
实验室提纯含有少量生石灰、泥沙的NaCl固体,进行如下提纯实验:
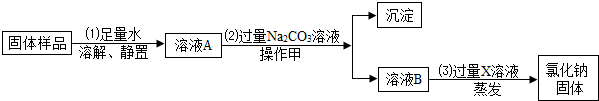
回答下列问题:
①溶液A中所含溶质为 (填化学式).
②加入Na2CO3溶液所发生反应的化学方程式为 .
③加入的过量X溶液作用是 .

回答下列问题:
①溶液A中所含溶质为
②加入Na2CO3溶液所发生反应的化学方程式为
③加入的过量X溶液作用是
考点:氯化钠与粗盐提纯,生石灰的性质与用途,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:①生石灰与水反应生成氢氧化钙,NaCl固体溶于水形成氯化钠溶液,泥沙难溶于水,据此进行分析解答.
②加入Na2CO3溶液,碳酸钠与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,写出反应的化学方程式即可.
③过滤后,溶液B为氯化钠、氢氧化钠、碳酸钠的混合溶液,加入X后得到氯化钠溶液,说明X溶液与氢氧化钠、碳酸钠发生反应生成了氯化钠,X应为是稀盐酸,据此进行分析解答.
②加入Na2CO3溶液,碳酸钠与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,写出反应的化学方程式即可.
③过滤后,溶液B为氯化钠、氢氧化钠、碳酸钠的混合溶液,加入X后得到氯化钠溶液,说明X溶液与氢氧化钠、碳酸钠发生反应生成了氯化钠,X应为是稀盐酸,据此进行分析解答.
解答:解:①生石灰与水反应生成氢氧化钙,NaCl固体溶于水形成氯化钠溶液,泥沙难溶于水,溶液A中所含溶质为氯化钠、氢氧化钙,其化学式分别是NaCl、Ca(OH)2.
②加入Na2CO3溶液,碳酸钠与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
③过滤后,溶液B为氯化钠、氢氧化钠、碳酸钠的混合溶液,加入X后得到氯化钠溶液,说明X溶液与氢氧化钠、碳酸钠发生反应生成了氯化钠,X应为是稀盐酸,目的是除尽B溶液中的氢氧化钠和碳酸钠.
故答案为:①NaCl、Ca(OH)2;②Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;③除尽B溶液中的氢氧化钠和碳酸钠.
②加入Na2CO3溶液,碳酸钠与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
③过滤后,溶液B为氯化钠、氢氧化钠、碳酸钠的混合溶液,加入X后得到氯化钠溶液,说明X溶液与氢氧化钠、碳酸钠发生反应生成了氯化钠,X应为是稀盐酸,目的是除尽B溶液中的氢氧化钠和碳酸钠.
故答案为:①NaCl、Ca(OH)2;②Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;③除尽B溶液中的氢氧化钠和碳酸钠.
点评:本题难度不大,掌握粗盐提纯的原理、盐的化学性质、生石灰的化学性质是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在给出的下列四个化学实验基本操作示意图中,你认为不正确的是( )
A、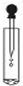 滴加液体 |
B、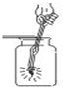 细铁丝在氧气中燃烧 |
C、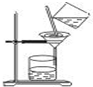 过滤 |
D、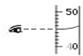 读量筒中液体的体积 |
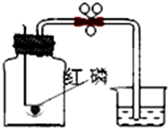 可用于测定空气中氧气的含量.实验前在集气瓶中加入少量水,并做上记号.下列说法中不正确的是( )
可用于测定空气中氧气的含量.实验前在集气瓶中加入少量水,并做上记号.下列说法中不正确的是( )| A、实验时红磷一定要过量 |
| B、点燃红磷前要先夹紧弹簧夹 |
| C、红磷熄灭后立即打开弹簧夹 |
| D、最终进入瓶中的水的体积约为氧气的体积 |
如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )
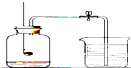

| A、红磷燃烧产生大量白色烟雾 | ||
| B、燃烧匙中的红磷可以换成细铁丝 | ||
| C、该实验可说明N2溶于水 | ||
D、红磷的量不足会导致进入集气瓶中水的体积小于
|
在下列实验操作(或措施)中,不正确的是( )
| A、用过氧化氢制氧气时,向过氧化氢溶液中加入少量MnO2-加快分解速率 |
| B、点燃氢气前,一定要先检验氢气的纯度-防止发生爆炸 |
| C、装NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞-防止溶液变质 |
| D、实验室储存白磷时,将其浸没在冷水中-防止发生自燃 |