题目内容
要得到8克氧气至少有多少摩尔双氧水?多少克双氧水?若有5%的双氧水溶液来制取这些氧气,需该溶液多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:此题是根据化学方程式计算的基本题型,主要是依靠已知物质的质量列出比例式求出未知物质的质量.
解答:解:
设需要双氧水的质量是x.
2H2O2
2H2O↑+O2↑
68 32
x 8g
=
x=17g
则双氧水的物质的量为
=0.5mol.
双氧水溶液的质量为:17g÷5%=340g.
答:至少有0.5摩尔双氧水,17克双氧水,需该溶液340克.
设需要双氧水的质量是x.
2H2O2
| ||
68 32
x 8g
| 68 |
| 32 |
| x |
| 8g |
x=17g
则双氧水的物质的量为
| 17g |
| 34g/mol |
双氧水溶液的质量为:17g÷5%=340g.
答:至少有0.5摩尔双氧水,17克双氧水,需该溶液340克.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
下列各物质在氧气中燃烧时,能发出明亮蓝紫色火焰的是( )
| A、木条 | B、木炭 | C、硫 | D、铁丝 |

 某厂排出的废液主要含硝酸锌和硝酸银,为了从回收金属银和硝酸锌,某中学化学课外活动组设计了以下的实验步骤:
某厂排出的废液主要含硝酸锌和硝酸银,为了从回收金属银和硝酸锌,某中学化学课外活动组设计了以下的实验步骤: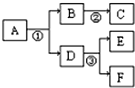 A~F是初中化学常见物质,相互转化关系如图:(部分反应物或生成物及反应条件略).
A~F是初中化学常见物质,相互转化关系如图:(部分反应物或生成物及反应条件略).