题目内容
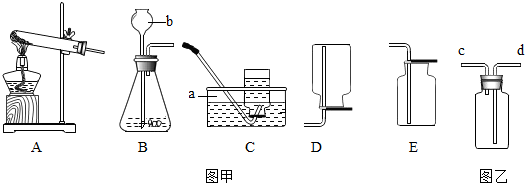
17. 实验室现有一种含有氯化钠的纯碱固体样品.某化学兴趣小组的同学在老师的指导下,利用如图所示装置(部分固定装置已略去)进行实验,测定其中纯碱的含量,并证实二氧化碳能与氢氧化钠发生化学反应.已知,该装置气密性良好,氢氧化钠溶液过量.
实验室现有一种含有氯化钠的纯碱固体样品.某化学兴趣小组的同学在老师的指导下,利用如图所示装置(部分固定装置已略去)进行实验,测定其中纯碱的含量,并证实二氧化碳能与氢氧化钠发生化学反应.已知,该装置气密性良好,氢氧化钠溶液过量.Ⅰ.称量纯碱样品质量记为m,装置B及其中试剂的总质量为m1,
Ⅱ.将质量为m的样品装入装置A中,关闭止水夹K2,打开止水夹K1.向样品中加入足量的稀硫酸,充分反应后,观察到C装置中的澄清石灰水不变浑浊.再次称B装置的总质量为m2.
Ⅲ.关闭止水夹K1,打开止水夹K2,使B装置与空气连通.向D装置内加入足量的稀盐酸(溶液浸没长颈漏斗下端管口)充分反应,观察现象.请回答:
(1)利用A装置制取二氧化碳的发生装置与实验室用氯酸钾制取氧气的发生装置不相同(填“相同”或“不同”)
(2)二氧化碳与氢氧化钠反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
(3)依据实验所得数据,该组甲同学得出计算样品中纯碱含量的式子为$\frac{53({m}_{2}-{m}_{1})}{22m}$,通过误差分析,乙同学发现所用数据不可靠.造成该数据不可靠的原因及其对计算结果的影响是:
①没有事先排走空气中的二氧化碳,导致计算结果偏大.
②装置内还有残留的二氧化碳气体没有被氢氧化钠溶液吸收,导致测量结果偏小.(任选一个因素)
(4)证实二氧化碳与氢氧化钠溶液发生了反应的现象是C中液体压入B中,产生白色沉淀.
(5)实验结束后,B装置溶液中含有的溶质可能有多种情况,任意写出其中的一种情况NaOH或NaOH、Ca(OH)2或NaOH、Na2CO3.
分析 (1)制取气体的实验装置取决于反应物的状态和反应的条件;
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
(3)根据实验的注意事项来分析产生误差的可能原因;
(4)根据装置内压强的变化以及碳酸钠与氢氧化钙反应的现象来分析;
(5)根据B装置中发生的反应来分析.
解答 解:(1)在实验室中,通常固态的大理石或石灰石与液态的稀盐酸反应来制取二氧化碳,而用加热氯酸钾固体的方法来制取氧气,故两套装置不相同;故填:不相同;
(2)氢氧化钠与二氧化碳反应生成碳酸钠和水,故填:CO2+2NaOH=Na2CO3+H2O;
(3)在实验过程中,必需保证生成的二氧化碳要被氢氧化钠溶液完全吸收,故填:装置内还有残留的二氧化碳气体没有被氢氧化钠溶液吸收,导致测量结果偏小.
(4)B装置中二氧化碳与氢氧化钠溶液反应,气体体积减小,造成该装置内气体的压强减小,会看到澄清的石灰水被吸入装置B,且与其中的碳酸钠反应生成了碳酸钙白色沉淀;故填:C中液体压入B中,产生白色沉淀.
(5)B装置中原来是氢氧化钠,和二氧化碳反应生成了碳酸钠,碳酸钠与氢氧化钙反应生成了氢氧化钠和碳酸钙沉淀.
故填:NaOH或NaOH、Ca(OH)2或NaOH、Na2CO3.
点评 本题考查了实验室中制取气体的装置、化学方程式的书写、实验误差的分析以及实验结论的分析,难度适中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.三亚硝酸氮[N(NO2)3]是一种新型火箭推进剂的原料.下列有关说法正确的是( )
| A. | N(NO2)3由三种元素组成 | B. | N(NO2)3属于有机化合物 | ||
| C. | N(NO2)3的相对分子质量为152 | D. | N(NO2)3中氮元素质量分数为56% |
8.下列叙述正确的是( )
| A. | 电动车充电是化学能转化为电能 | |
| B. | 生活中常用过滤的方法将硬水转化成软水 | |
| C. | 洗涤剂具有乳化功能,可以去除餐具上的油污 | |
| D. | 不吃水果蔬菜,多吃含蛋白质的肉类,更能增强体质 |
6.下列物质的用途主要由化学性质决定的是( )
| A. | 用氧气抢救病人 | B. | 铜丝用作导线 | ||
| C. | 金刚石切割玻璃 | D. | 用活性炭吸附有色物质 |