题目内容
12.请你协助小明配制100克质量分数为20%氯化钠的溶液.(1)需要氯化钠为20 克,水为80 毫升;
(2)小明的操作见下图所示.正确的操作步骤应是④⑤①②③ (填写数字序号);
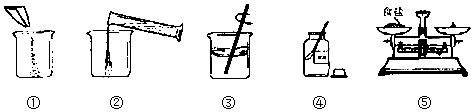
(3)会导致所得氯化钠溶液溶质质量分数偏小的原因有哪些?AC(填写字母)
A.氯化钠中有杂质 B.称量时使用了生锈的砝码
C.用量筒量取水时,仰视读数 D.配制完成后移取液体时有部分溅出.
分析 (1)溶质质量=溶液质量×溶质质量分数;
(2)正确的操作步骤应是:取出药品,称量药品质量,把药品放入烧杯中,量取水倒入烧杯中,利用玻璃棒搅拌使药品完全溶解;
(3)A.氯化钠中有杂质时,会导致氯化钠质量偏小,从而导致配制溶液质量分数偏小;
B.称量时使用了生锈的砝码,会导致氯化钠质量偏大,从而导致配制溶液质量分数偏大;
C.用量筒量取水时,仰视读数,会导致量取水的体积偏大,从而导致配制溶液质量分数偏小;
D.配制完成后移取液体时有部分溅出,不影响溶液的溶质质量分数.
解答 解:(1)需要氯化钠为:100g×20%=20g,需要水的体积为:(100g-20g)÷1g/mL=80mL.
故填:20;80.
(2)正确的操作步骤应是:取出药品,称量药品质量,把药品放入烧杯中,量取水倒入烧杯中,利用玻璃棒搅拌使药品完全溶解.
故填:④⑤①②③.
(3)A.氯化钠中有杂质时,会导致氯化钠质量偏小,从而导致配制溶液质量分数偏小;
B.称量时使用了生锈的砝码,会导致氯化钠质量偏大,从而导致配制溶液质量分数偏大;
C.用量筒量取水时,仰视读数,会导致量取水的体积偏大,从而导致配制溶液质量分数偏小;
D.配制完成后移取液体时有部分溅出,不影响溶液的溶质质量分数.
故填:AC.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
4.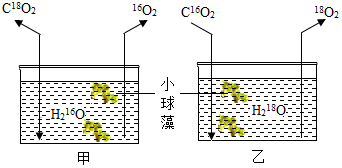 过去人们一直对于光合作用产物O2的来源感到疑惑.现科学家利用中子数不同的两种氧原子18O和16O标记水和二氧化碳分子中的氧原子,进行了如图实验.请你判断光合作用产生的O2来自( )
过去人们一直对于光合作用产物O2的来源感到疑惑.现科学家利用中子数不同的两种氧原子18O和16O标记水和二氧化碳分子中的氧原子,进行了如图实验.请你判断光合作用产生的O2来自( )
 过去人们一直对于光合作用产物O2的来源感到疑惑.现科学家利用中子数不同的两种氧原子18O和16O标记水和二氧化碳分子中的氧原子,进行了如图实验.请你判断光合作用产生的O2来自( )
过去人们一直对于光合作用产物O2的来源感到疑惑.现科学家利用中子数不同的两种氧原子18O和16O标记水和二氧化碳分子中的氧原子,进行了如图实验.请你判断光合作用产生的O2来自( )| A. | CO2 | B. | H2O | ||
| C. | 部分来自CO2,部分来自H2O | D. | 无法判断 |
17.粗盐精制是为了除去粗盐中的MgCl2、CaCl2、Na2SO4及泥沙等杂质,为了保证杂质除得彻底,精制时所加除杂试剂一般要过量,而多出的除杂试剂则应在后续步骤中除去,因此必须考虑先后顺序.粗盐精制的方法如下:a.加入稍过量的NaOH;b.加入稍过量的Na2CO3;c.加入稍过量的BaCl2;d.加入适量的HCl;e.过滤.其中正确的顺序是( )
| A. | abcde | B. | baced | C. | cabed | D. | cbaed |
4.某同学对气体的实验室制法作了以下探究,请根据图1回答下列问题:
(1)写出标有序号的仪器的名称.

a分液漏斗;b水槽.
〔2〕如果要在实验室制取二氧化碳,则应该选择的装置组合为AD(填字母),不能用C装置收集气体的理由是:二氧化碳能溶于水(请用文字说明).
〔3〕若某兴趣小组同学用以上某装置对实验室制备氧气的条件进行如下探究实验.
①为探究催化剂的种类对氯酸钾分解速度的影响,甲同学设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;Ⅱ中x的值应为3.0.
②乙同学探究了影响双氧水分解速度的某种因素.实验数据记录如下:
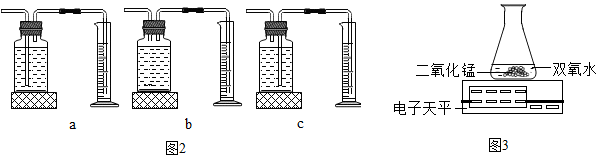
本实验中,测量O2体积的装置是c(填图2编号).实验结论:在相同条件下,双氧水中溶质的质量分数越 大(填“大”或“小”),双氧水分解得越快.
丙同学用图3装置进行实验也能达到实验目的,其还需要的实验仪器是②(填编号)
①温度计 ②计时器 ③密度计 ④刻度尺.
(1)写出标有序号的仪器的名称.

a分液漏斗;b水槽.
〔2〕如果要在实验室制取二氧化碳,则应该选择的装置组合为AD(填字母),不能用C装置收集气体的理由是:二氧化碳能溶于水(请用文字说明).
〔3〕若某兴趣小组同学用以上某装置对实验室制备氧气的条件进行如下探究实验.
①为探究催化剂的种类对氯酸钾分解速度的影响,甲同学设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;Ⅱ中x的值应为3.0.
②乙同学探究了影响双氧水分解速度的某种因素.实验数据记录如下:
| 双氧水的质量 | 双氧水中溶质的质量分数 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |

本实验中,测量O2体积的装置是c(填图2编号).实验结论:在相同条件下,双氧水中溶质的质量分数越 大(填“大”或“小”),双氧水分解得越快.
丙同学用图3装置进行实验也能达到实验目的,其还需要的实验仪器是②(填编号)
①温度计 ②计时器 ③密度计 ④刻度尺.
1.下列说法错误的是( )
| A. | 纯碱不是碱 | B. | 氢氧化钠固体用于干燥CO2 | ||
| C. | 碳酸氢钠用于治疗胃酸过多 | D. | 碳酸不属于有机物 |
2.氯化铵(NH4Cl)是农田化肥中的一种,过量使用会造成土壤污染.已知Cl元素为-1价,氯化铵中氮元素的化合价为( )
| A. | -3 | B. | 0 | C. | +3 | D. | +5 |
