题目内容
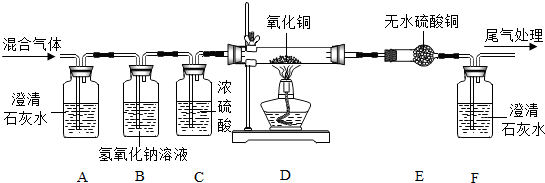
利用化学反应中气体产生的压力,可使多个化学反应依次发生.如图所示,装置气密性良好,A~F中盛放的物质分别为:A. 氯酸钾与少量二氧化锰的混合物;B. 足量稀酸溶液;C.某难溶固体;D.滴有紫色石蕊试液的蒸馏水;E.澄清石灰水;F.水.点燃酒精灯加热A时,多个反应能够从左向右依次发生.

(1)写出图中仪器的名称:a ,b .
(2)A中产生的气体是 ,该反应的类型为 反应.
(3)实验过程中,D中液体变为红色,E中溶液由澄清变浑浊.则B、C中的原物质是:B ,C .
(4)写出D、E中发生反应的化学方程式: ; .
(5)若选用装置F收集氧气(F盛满水),则氧气应从导管 (选填①或②)通入.
(6)氨气是一种无色、有刺激性气味、密度比空气小、极易溶于水的气体,实验室里用加热氯化铵(NH4Cl)和氢氧化钙的固体混合物的方法制取氨气,同时生成氯化钙和水,则实验室收集氨气应用 法;请写出该反应的化学方程式: .

(1)写出图中仪器的名称:a
(2)A中产生的气体是
(3)实验过程中,D中液体变为红色,E中溶液由澄清变浑浊.则B、C中的原物质是:B
(4)写出D、E中发生反应的化学方程式:
(5)若选用装置F收集氧气(F盛满水),则氧气应从导管
(6)氨气是一种无色、有刺激性气味、密度比空气小、极易溶于水的气体,实验室里用加热氯化铵(NH4Cl)和氢氧化钙的固体混合物的方法制取氨气,同时生成氯化钙和水,则实验室收集氨气应用
考点:氧气的制取装置,二氧化碳的化学性质,酸的化学性质,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据实验室常用仪器解答;
(2)根据已有的知识进行分析,氯酸钾在二氧化锰的催化作用下,加热能快速分解产生氧气,根据反应物和生成物的种类特点能确定反应的类型;
(3)根据紫色石蕊试液遇酸变红,A中产生的氧气使装置压强增大,将B中的液体导入C,与C中的物质混合产生气体,进入D,D中液体变红,则D中盛有的是石蕊试液,说明B中盛有的是盐酸,C中盛有的是碳酸钙,反应生成二氧化碳,二氧化碳能使石灰水变浑浊解答;
(4)根据二氧化碳和水反应生成碳酸,二氧化碳能使石灰水变浑浊,写出反应的方程式;
(5)根据氧气的密度比水的密度小解答;
(6)实验室用氯化铵和氢氧化钙在加热条件下制备氨气,利用固体+固体加热制备气体选择气体发生装置,根据氨气是易溶于水的比空气轻的气体选择收集装置;
(2)根据已有的知识进行分析,氯酸钾在二氧化锰的催化作用下,加热能快速分解产生氧气,根据反应物和生成物的种类特点能确定反应的类型;
(3)根据紫色石蕊试液遇酸变红,A中产生的氧气使装置压强增大,将B中的液体导入C,与C中的物质混合产生气体,进入D,D中液体变红,则D中盛有的是石蕊试液,说明B中盛有的是盐酸,C中盛有的是碳酸钙,反应生成二氧化碳,二氧化碳能使石灰水变浑浊解答;
(4)根据二氧化碳和水反应生成碳酸,二氧化碳能使石灰水变浑浊,写出反应的方程式;
(5)根据氧气的密度比水的密度小解答;
(6)实验室用氯化铵和氢氧化钙在加热条件下制备氨气,利用固体+固体加热制备气体选择气体发生装置,根据氨气是易溶于水的比空气轻的气体选择收集装置;
解答:解:
(1)根据实验室常用仪器可知a试管;b酒精灯;
(2)氯酸钾在二氧化锰的催化作用下,加热能快速分解产生氧气,此反应为分解反应,故填:2KClO3
2KCl+3O2↑,分解;
(3)紫色石蕊试液遇酸变红,A中产生的氧气使装置压强增大,将B中的液体导入C,与C中的物质混合产生气体,进入D,D中液体变红,则D中盛有的是石蕊试液,说明B中盛有的是盐酸,C中盛有的是碳酸钙,反应生成二氧化碳,二氧化碳能使石灰水变浑浊,故E中生成的是碳酸钙,故填:盐酸,碳酸钙.
(4)二氧化碳和水反应生成碳酸,反应的方程式为:CO2+H2O=H2CO3 ;二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(5)氧气的密度比水的密度小,选用装置F收集氧气(F盛满水),则氧气应从导管②进;
(6)氨气是易溶于水的比空气轻的气体,需要用向下排空气方法收集氨气;
实验室用氢氧化钙和氯化铵在加热条件下制备氨气,反应方程式为2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑.
答案:
(1)a试管;b酒精灯;
(2)2KClO3
2KCl+3O2↑,
(3)盐酸,碳酸钙.
(4)CO2+H2O=H2CO3 ;Ca(OH)2+CO2=CaCO3↓+H2O;
(5)②
(6)向下排空气 2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑.
(1)根据实验室常用仪器可知a试管;b酒精灯;
(2)氯酸钾在二氧化锰的催化作用下,加热能快速分解产生氧气,此反应为分解反应,故填:2KClO3
| ||
| △ |
(3)紫色石蕊试液遇酸变红,A中产生的氧气使装置压强增大,将B中的液体导入C,与C中的物质混合产生气体,进入D,D中液体变红,则D中盛有的是石蕊试液,说明B中盛有的是盐酸,C中盛有的是碳酸钙,反应生成二氧化碳,二氧化碳能使石灰水变浑浊,故E中生成的是碳酸钙,故填:盐酸,碳酸钙.
(4)二氧化碳和水反应生成碳酸,反应的方程式为:CO2+H2O=H2CO3 ;二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(5)氧气的密度比水的密度小,选用装置F收集氧气(F盛满水),则氧气应从导管②进;
(6)氨气是易溶于水的比空气轻的气体,需要用向下排空气方法收集氨气;
实验室用氢氧化钙和氯化铵在加热条件下制备氨气,反应方程式为2NH4Cl+Ca(OH)2
| ||
答案:
(1)a试管;b酒精灯;
(2)2KClO3
| ||
| △ |
(3)盐酸,碳酸钙.
(4)CO2+H2O=H2CO3 ;Ca(OH)2+CO2=CaCO3↓+H2O;
(5)②
(6)向下排空气 2NH4Cl+Ca(OH)2
| ||
点评:此题考查了常见物质的性质,完成此题,可以依据已有的物质的性质进行,要求同学们加强对基础知识的储备,以便灵活应用.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
如图是三种微粒的结构示意图,有关它们的说法正确的是( )


| A、它们都是原子 |
| B、它们的核外都有两个电子层 |
| C、它们是属于同种元素的微粒 |
| D、它们的最外层电子数不同 |
下列物质中属于纯净物的是( )
| A、氯酸钾 | B、汽油 |
| C、新鲜的空气 | D、矿泉水 |
只用一种试剂就能将NaOH、NaCl、BaCl2三种溶液鉴别出来,它是( )
| A、酚酞溶液 | B、硫酸钠溶液 |
| C、硫酸铜溶液 | D、硝酸铁溶液 |