题目内容
17.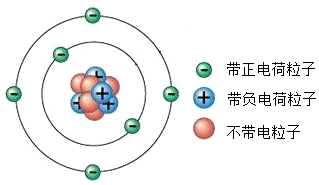 如图为某原子的结构示意图
如图为某原子的结构示意图(1)该原子的原子核中有6个质子.
(2)与原子的化学性质关系最密切的是最外层电子数.
(3)该原子与氧原子结合形成的物质是空气的组成成分之一,检验该化合物的常用方法是通入澄清石灰水,如果变浑浊,则为二氧化碳,用化学方程式表达是CO2+Ca(OH)2=CaCO3↓+H2O.
分析 (1)根据在原子中质子数等电子数分析判断;
(2)根据原子的性质与最外层电子数的关系分析;
(3)根据二氧化碳的性质分析回答.
解答 解:(1)在原子中质子数等电子数,该原子的原子核中6个质子;
(2)与原子的化学性质关系最密切的是最外层电子数.
(3)该原子的质子数是6,是碳原子,与氧原子结合形成的物质是空气的组成成分之一的二氧化碳,检验该化合物的常用方法是通入澄清石灰水,如果变浑浊,则为二氧化碳,用化学方程式表达是:CO2+Ca(OH)2=CaCO3↓+H2O.
故答为:(1)6;(2)最外层电子数;(3)通入澄清石灰水,如果变浑浊,则为二氧化碳,CO2+Ca(OH)2=CaCO3↓+H2O.
点评 本题的难度不大,了解原子结构示意图的意义和二氧化碳的性质是解答本题的关键.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
7.地壳中含量最多的金属元素与非金属元素和空气中含量最多的元素,三种元素可以组成的物质是( )
| A. | CaCO3 | B. | Fe(OH)3 | C. | Al(NO3)3 | D. | Fe(NO3)3 |
5.NaCl和KNO3在不同温度时的溶解度如表:
下列说法正确的是( )
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| A. | 10℃时,将40g NaCl固体加入l00g水中,可得到l40gNaCl溶液 | |
| B. | 40℃KNO3溶液溶质质量分数一定比NaCl溶液溶质质量分数大 | |
| C. | 将30℃的KNO3饱和溶液升温至60℃,会变成不饱和溶液 | |
| D. | 20℃时,NaCl饱和溶液的溶质质量分数为36% |
6.下列能源不属于化石燃料的是( )
| A. | 煤 | B. | 石油 | C. | 酒精 | D. | 天然气 |
7.化学用语是学习化学的重要工具,是国际通用的化学语言.
(1)请在下表空白处填上适当的内容:
(2)写出下列反应的化学方程式,并注明基本反应类型:
①镁和稀硫酸反应Mg+H2SO4=MgSO4+H2↑,属于置换反应;
②碳酸钠溶液与澄清石灰水混合Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,属于复分解反应.
(1)请在下表空白处填上适当的内容:
| 物质名称 | 镁 | 熟石灰 | ||
| 化学式 | N2 | |||
| 构成物质的微粒符号 | K+、SO42- |
①镁和稀硫酸反应Mg+H2SO4=MgSO4+H2↑,属于置换反应;
②碳酸钠溶液与澄清石灰水混合Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,属于复分解反应.
 探究活动一:在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.
探究活动一:在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.