题目内容
20.硫酸铜(化学式:CuSO4 ),为白色或灰白色粉末,易跟水反应生成蓝色的五水合硫酸铜(化学式为:CuSO4•5H2O)(俗称胆矾或蓝矾)(1)硫酸铜的物理性质有白色或灰白色粉末(写一点),硫酸铜属于(“酸”“碱”“盐”或“氧化物”)中的盐
(2)硫酸铜中铜元素和硫元素的质量比是2:1,铜元素的质量分数是40%
(3)实验室用硫酸铜晶体(化学式为:CuSO4•5H2O)配制100g8%的硫酸铜溶液,需称取硫酸铜晶体12.5g.
分析 (1)根据题干信息和硫酸铜的组成分析,
(2)据元素质量比=相对原子质量与相应原子个数的乘积比,纯净物中某元素的质量分数=$\frac{元素的相对原子质量×原子个数}{相对分子质量}$×100%,进行分析.
(3)利用溶质质量=溶液质量×溶质的质量分数,硫酸铜晶体是CuSO4•5H2O,进行分析解答.
解答 解:(1)硫酸铜为白色或灰白色粉末,属于物理性质,硫酸铜有铜离子和硫酸根离子构成,属于盐;故填:白色或灰白色粉末;盐;
(2)硫酸铜中铜元素和硫元素的质量比为64:32=2:1.硫酸铜中铜元素的质量分数=$\frac{64}{64+32+16×4}$×100%=40%;故填:2:1;40%;
(3)用溶质质量=溶液质量×溶质的质量分数,配制100g16%的硫酸铜溶液,需要硫酸铜的质量为100g×8%=8g;则需要硫酸铜晶体的质量为8g÷($\frac{64+32+16×4}{64+32+16×4+(1×2+16)×5}$×100%)=12.5g.故填:12.5g.
点评 本题难度不大,掌握溶质质量分数的有关计算、化学式的有关计算并能灵活运用是正确解答本题的关键.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
11.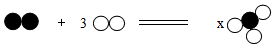 如图是某化学反应的微观模型,“○”“
如图是某化学反应的微观模型,“○”“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
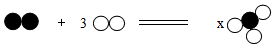 如图是某化学反应的微观模型,“○”“
如图是某化学反应的微观模型,“○”“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )| A. | 该反应属于分解反应 | |
| B. | 图示中x值为6 | |
| C. | 参加反应的两种物质质量之比为1:3 | |
| D. | 反应中有两种元素化合价发生变化 |
8.下列实验操作、现象与结论对应关系不正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用黄铜片在铜片上刻画 | 铜片上有划痕 | 黄铜的硬度比铜大 |
| B | 将两根铁丝分别伸到CuSO4溶液和AgNO3溶液中 | 两根铁丝表面均有固体附着 | 金属的活动性是Fe>Cu>Ag |
| C | 向某溶液中滴入无色酚酞试液 | 无色酚酞试液不变色 | 无色溶液不一定是酸 |
| D | 向某物质加入稀硫酸 | 有气泡产生 | 该物质可能含有CO32- |
| A. | A | B. | B | C. | C | D. | D |
5.下列化学符号表示两个分子的是( )
| A. | 2H | B. | 2CO | C. | SO42- | D. | SO2 |
12.化学世界绚丽多彩,下列实验中有关颜色的描述不正确的是( )
| A. | 硫粉在氧气中燃烧出现蓝紫色火焰 | |
| B. | 将铁钉加入到稀硫酸中,溶液由无色变为黄色 | |
| C. | 对木炭和氧化铜的粉末加强热会出现红色物质 | |
| D. | 将铜片放入硝酸银溶液,溶液由无色变为蓝色 |
9.在一定条件下,一密闭容器内发生某反应,测得反应前后各物质的质量如表所示,下列说法错误的是( )
| 物质 | a | b | c | d |
| 反应前的质量/g | 30 | 5 | 10 | 15 |
| 反应后的质量/g | x | y | 20 | 20 |
| A. | a一定是反应物 | B. | x+y=20 | ||
| C. | x的取值范围一定是0≤x≤30 | D. | 反应生成c与d的质量比为2:1 |

 ”、“
”、“ ”、“
”、“ ”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用.
”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用.