题目内容
8. 雨、雪在形成和降落过程中吸收、溶解了空气中SO2及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨,请回答下列有关酸雨的问题:
雨、雪在形成和降落过程中吸收、溶解了空气中SO2及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨,请回答下列有关酸雨的问题:(1)要测定某地采集到的雨水是否为酸雨,下列提供的试剂(试纸)中宜取用D
A.蓝色石蕊试纸 B.紫色石蕊溶液 C.无色酚酞试剂 D.pH试纸
(2)已知自然条件下形成的CO2溶液常温下pH不会小于 5.6.通常空气中CO2的含量大于 SO2的含量,但人们反而将空气中的 SO2认定为形成酸雨的主要原因之一.有同学想通过如图的实验寻找证据,你认为下一步的实验步骤是测定实验后水溶液的PH值,只要出现PH值小于5.6的实验结果,就可认定SO2溶于水有形成酸雨的可能.
分析 (1)依据酸雨是pH小于5.6的降水可知要想证明是否是酸雨则要测定溶液的pH,据此分析即可.
(2)依据题干信息结合设计的实验可知,只要是证明亚硫酸的溶液pH能小于5.6即可完成相关的验证.
解答 解:(1)因为酸雨是pH小于5.6的降水,所以要想证明是否是酸雨则要测定溶液的pH.
A、蓝色石蕊试纸是检验溶液酸性时常用的试纸,不能准确测量溶液酸碱度;
B、紫色石蕊溶液只能检验溶液的酸碱性,不能检测溶液的酸碱度;
C、无色酚酞试剂只能检验溶液的酸碱性,不能检测溶液的酸碱度
D、pH试纸能较准确地测量溶液的酸碱强弱的程度,所以检验某地是否下酸雨可利用pH试纸进行测量;
(2)二氧化硫溶于水会生成亚硫酸,二氧化碳溶于水会生成碳酸,而CO2的饱和溶液常温下pH不小于 5.6,所以要想证明二氧化硫是形成酸雨的主要成分,只要证明实验中亚硫酸的溶液pH能小于5.6即可.
答案:(1)D (2)实验后水溶液的PH值 PH值小于5.6
点评 此题是一道与酸雨相关的考查题,涉及到酸雨的形成及实验验证,借助题干信息结合相关的所学知识是解题的关键所在.

练习册系列答案
相关题目
18.下列有关CO2和CO的知识归纳,错误的是( )
| A. | 组成:1个二氧化碳分子比1个一氧化碳分子多1个氧原子 | |
| B. | 性质:都是无色无味的气体;都能溶于水,都能燃烧 | |
| C. | 用途:CO2用于灭火,“干冰”可用于人工降雨等;CO可作燃料、冶炼金属等 | |
| D. | 危害:CO2会造成“温室效应”;CO极易与血液中的血红蛋白结合引起中毒 |
16.工业上利用太阳能进行海水晒盐.已知海水蒸发浓缩过程中析出盐的种类和质量如下表:(表中数据为每升海水在浓缩过程中析出各种盐的质量,单位为g)
(1)海水从密度为1.21g•mL-1浓缩到1.22g•mL-1时发生的变化是C.
A.各种盐的溶解度增大 B.海水中水的质量分数不变
C.析出粗盐中NaCl的质量分数增大 D.海水中Br-的质量分数不变
(2)海水在浓缩过程中,最先析出的盐是硫酸钙.实际晒盐生产中,海水的密度一般控制在1.21g•mL-1~1.26g•mL-1范围内.由上表可知,所得粗盐中含有的杂质离子有Ca2+,Mg2+,SO42-;Br-.
(3)如图能较正确地反映浓缩过程中海水中NaCl的质量分数(A%)与海水密度(d)的关系的是B.

| 海水密度/(g•mL-1) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
| 1.13 | 0.56 | ||||
| 1.20 | 0.91 | ||||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 | |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
| 1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
A.各种盐的溶解度增大 B.海水中水的质量分数不变
C.析出粗盐中NaCl的质量分数增大 D.海水中Br-的质量分数不变
(2)海水在浓缩过程中,最先析出的盐是硫酸钙.实际晒盐生产中,海水的密度一般控制在1.21g•mL-1~1.26g•mL-1范围内.由上表可知,所得粗盐中含有的杂质离子有Ca2+,Mg2+,SO42-;Br-.
(3)如图能较正确地反映浓缩过程中海水中NaCl的质量分数(A%)与海水密度(d)的关系的是B.

3.在科学学习过程中,常常要用到分类的方法.下列各组物质的分类正确的是( )
| A. | 混合物:空气 粗盐 牛奶 | B. | 盐:氯化钙 硫酸 硝酸钾 | ||
| C. | 氧化物:MgO P2O5 KClO3 | D. | 单质:铝 金刚石 氯化氢 |
20.配制硝酸钾溶液时得到下表数据,根据表中数据分析,不正确的是( )
| 序号 | 温度/℃ | 水的质量/克 | 所加硝酸钾的质量/克 | 所得溶液的质量/克 |
| ① | 28 | 10 | 4 | 14 |
| ② | 28 | 10 | 6 | 14 |
| ③ | 60 | 10 | 8 | 18 |
| A. | ①②所得溶液溶质的质量分数相等 | |
| B. | ③所得溶液一定是硝酸钾的饱和溶液 | |
| C. | 28℃时10克水中最多能溶解硝酸钾4克 | |
| D. | 60℃时等质量水中能溶解的硝酸钾比28℃时多 |
17.把金属X放入CuSO4溶液中,X表面有红色固体析出;若放入FeSO4溶液中,无明显现象. 则X、Cu、Fe三种金属活动性由强到弱的顺序正确的是( )
| A. | Fe、X、Cu | B. | X、Fe、Cu | C. | Fe、Cu、X | D. | Cu、X、Fe |
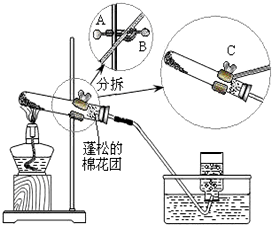 某同学做“高锰酸钾制取氧气”的实验过程如下:
某同学做“高锰酸钾制取氧气”的实验过程如下: