题目内容
钢铁是使用最多的金属材料.
(1)人类向大自然提取量最大的金属是铁.写出高温下一氧化碳把铁从赤铁矿石中还原出来的化学方程式 .
(2)锰(Mn)钢属于铁合金,可用于制造钢轨.取少量锰钢碎屑加入盛有足量稀盐酸的烧杯中,浸泡以后烧杯底部剩有固体,该固体中一定含有 .已知锰的金属活动性强于锌,如果用实验比较铁和锰的金属活动性强弱,下列所给试剂组能够达到目的是 (填序号).
A.Fe、Mn、40%H2SO4溶液 B.Fe、Mn、MgSO4溶液
C.Fe、Mn、ZnSO4溶液 D.Cu、FeSO4溶液、MnSO4溶液.
(1)人类向大自然提取量最大的金属是铁.写出高温下一氧化碳把铁从赤铁矿石中还原出来的化学方程式
(2)锰(Mn)钢属于铁合金,可用于制造钢轨.取少量锰钢碎屑加入盛有足量稀盐酸的烧杯中,浸泡以后烧杯底部剩有固体,该固体中一定含有
A.Fe、Mn、40%H2SO4溶液 B.Fe、Mn、MgSO4溶液
C.Fe、Mn、ZnSO4溶液 D.Cu、FeSO4溶液、MnSO4溶液.
考点:铁的冶炼,金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)赤铁矿的主要成分是氧化铁,在高温的条件下能被一氧化碳还原;
(2)根据铁合金中含有少量的碳以及验证金属活动性的方法来分析解答.
(2)根据铁合金中含有少量的碳以及验证金属活动性的方法来分析解答.
解答:解:(1)在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,其化学方程式为:Fe2O3+3CO
2Fe+3CO2;
(2)铁合金中含有少量的碳,与稀盐酸不发生反应;根据题干信息,锰的活动性大于锌,故可选择C来验证铁和锰的活动性:铁不能置换出硫酸锌中的锌,说明铁不如锌活泼,锰能置换出硫酸锌中的锌,说明锰比锌活泼,故活动性:锰>锌>铁.
故答案为:(1)Fe2O3+3CO
2Fe+3CO2;(2)C(或碳);C.
| ||
(2)铁合金中含有少量的碳,与稀盐酸不发生反应;根据题干信息,锰的活动性大于锌,故可选择C来验证铁和锰的活动性:铁不能置换出硫酸锌中的锌,说明铁不如锌活泼,锰能置换出硫酸锌中的锌,说明锰比锌活泼,故活动性:锰>锌>铁.
故答案为:(1)Fe2O3+3CO
| ||
点评:本题难度不是很大,主要考查铁的冶炼以及对金属活动性顺序的应用,从而培养学生对知识的灵活运用.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
下列实验现象描述正确的是( )
| A、木炭在氧气中剧烈燃烧,发出白光,生成有刺激性气味的气体 |
| B、细铁丝在空气中燃烧,火星四射,生成黑色固体 |
| C、红磷在空气中燃烧,产生大量的白雾 |
| D、电解水实验中正极产生气体与负极产生气体的体积比为1:2 |
鉴别O2、CO、CO2三种气体,简便可行的方法是( )
| A、将气体分别通入澄清石灰水 |
| B、将气体分别通入石蕊试液 |
| C、将三种气体分别通入水 |
| D、用燃着的木条分别伸入集气瓶内 |
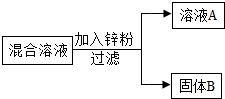 金属具有广泛的应用,根据金属及其化合物的性质和用途,请回答:
金属具有广泛的应用,根据金属及其化合物的性质和用途,请回答: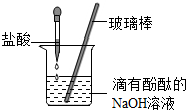 盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,初中化学中许多实验都用到了盐酸.
盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,初中化学中许多实验都用到了盐酸.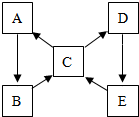 几种常见物质之间的相互转化关系如图所示(各字母代表一种物质,部分反应物、生成物及反应条件略去)己知:①五种物质均含铜元素,且化合物中铜元素的化合价均为+2; ②B为黑色固体物质; ③C溶液与铁反应可得到A; ④C溶液与氯化钡溶液反应可得到D,同时有白色沉淀生成; ⑤D溶液中加入少量的氢氧化钠溶液得到E.结合信息推断:
几种常见物质之间的相互转化关系如图所示(各字母代表一种物质,部分反应物、生成物及反应条件略去)己知:①五种物质均含铜元素,且化合物中铜元素的化合价均为+2; ②B为黑色固体物质; ③C溶液与铁反应可得到A; ④C溶液与氯化钡溶液反应可得到D,同时有白色沉淀生成; ⑤D溶液中加入少量的氢氧化钠溶液得到E.结合信息推断: 2012年9月25日,我国第一艘航空母舰“辽宁号”正式入列.这对于我国捍卫国家主权,维护领土完整具有重要意义,如图为“辽宁号”实物图,请回答下列问题.
2012年9月25日,我国第一艘航空母舰“辽宁号”正式入列.这对于我国捍卫国家主权,维护领土完整具有重要意义,如图为“辽宁号”实物图,请回答下列问题.