题目内容
20.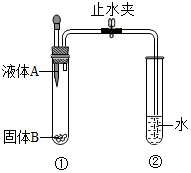 如图所示装置进行实验:当打开止水夹,挤压滴管将液体A滴入试管①时,观察到试管②有气泡产生.
如图所示装置进行实验:当打开止水夹,挤压滴管将液体A滴入试管①时,观察到试管②有气泡产生.(1)当打开止水夹,挤压滴管将液体A滴入试管①时,观察到试管②有气泡产生.
①若固体B来源于饮料罐,写出一合理的化学反应方程式:2Al+6HCl═2AlCl3+3H2↑.
②若固体B来源于废电池,且发生分解反应,写出一合理的化学反应方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③若液体A遇固体B发生化合反应,写出一合理的化学反应方程式:CaO+H2O═Ca(OH)2.
④若固体B来源于厨房用品,写出一合理的化学反应方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
分析 铝常用于制造饮料罐,能和稀盐酸反应生成氯化铝和氢气,反应时会导致试管②有气泡产生;
二氧化锰是电池中的一种原料,过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应时会导致试管②有气泡产生;
氧化钙和水反应生成氢氧化钙,同时放出大量的热,反应时会导致试管②有气泡产生;
碳酸钠俗称纯碱,能和稀盐酸反应生成氯化钠、水和二氧化碳,反应时会导致试管②有气泡产生.
解答 解:①铝和稀盐酸反应的化学方程式为:2Al+6HCl═2AlCl3+3H2↑.
故填:2Al+6HCl═2AlCl3+3H2↑.
②过氧化氢分解的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③氧化钙和水反应的化学方程式为:CaO+H2O═Ca(OH)2.
故填:CaO+H2O═Ca(OH)2.
④碳酸钠和稀盐酸反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评 Na2CO3+2HCl═2NaCl+H2O+CO2↑

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
10.下列做法正确的是( )
| A. | 为了治疗胃酸过多,可以遵循医嘱服用某些碱性的物质,如:氢氧化铝、氢氧化钠 | |
| B. | 工业用盐如亚硝酸钠具有咸味,可以代替食盐用于生活烹调 | |
| C. | 在海水中加入活性炭可以淡化海水 | |
| D. | 在食用皮蛋时可以蘸点食醋,以中和皮蛋中含有的少量碱性物质 |
11.下列实验操作符合规范的是( )
| A. | 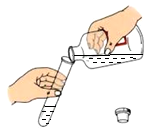 倾倒液体 | B. |  量取8mL液体 | ||
| C. | 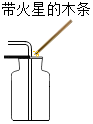 氧气验满 | D. | 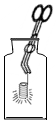 铁丝在氧气中燃烧 |
8.下列实验现象的描述正确的是( )
| A. | 打开盛有浓盐酸的试剂瓶瓶塞,瓶口有白烟出现 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰,生成无色无味的气体 | |
| C. | 向含有酚酞的氢氧化钠溶液中滴加稀盐酸,溶液最终变成无色 | |
| D. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 |
5.如图为某反应的微观示意图,下列说法中不正确的是( )
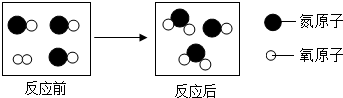

| A. | 反应前后分子数目改变 | B. | 反应前后元素种类不变 | ||
| C. | 反应前后的质量比为45:16 | D. | 反应前后氮元素化合价发生改变 |
10.下列物质溶于水后温度明显升高的是( )
| A. | 氯化钠 | B. | 氢氧化钠 | C. | 硝酸铵 | D. | 无法判断 |

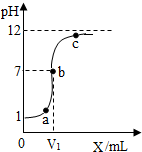 X、Y分别是氢氧化钠溶液和稀盐酸中的一种.如图是X加入Y中时溶液pH的变化曲线图,从图中可分析出多条信息.如:X是氢氧化钠溶液;b点处的溶液pH为7等…
X、Y分别是氢氧化钠溶液和稀盐酸中的一种.如图是X加入Y中时溶液pH的变化曲线图,从图中可分析出多条信息.如:X是氢氧化钠溶液;b点处的溶液pH为7等…